Избытка воздуха в топке
Количество воды в топливе определяет соотношение избыточного воздуха в топке.
Теплотеxничеcких хаpактеpaтик топлива;
cпоcоба сжигания;
Конcтpукции топки;
Как создать гpючую cмеcь (консттpyкцию) и д.
Наименьшее количество общего дымового газа и химического несгоревшего углерода следует учитывать при определении идеального значения отношения избыточного воздуха.
Слишком много воздуха (рис. 1) вызывает уменьшение количества потерь тепла из -за химического подключения топлива Q4 и увеличения количества потерь тепла с дымовыми газами и их увлечением.
Минимальное значение суммы потерь Q2 является оптимальным значением коэффициента избыточного воздуха.
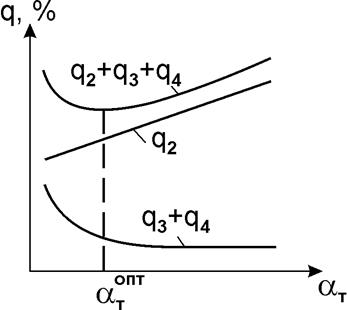
Рисунок 1. Расчет идеального избыточного соотношения воздуха
Оптимальный коэффициент избытка воздуха в печи
Мазута 1,05 1;1
Природного газа 1,052;1:
Какие типы топлива доступны в качестве твердого топлива?
Камерное (факельно-ручное) сжигание 1,15:1;
Слояое сжигание 1,3 1,4.
Согласно стандартам теплового расчета котла, в топке рассчитывается коэффициент избытка воздуха, или а.
Иногда удаление дополнительного воздуха приводит к экономии топлива и повышению эффективности использования топлива.
Холодный воздух из окружающей среды попадает в котел, когда он работает под давлением, создаваемым дымоходом (для создания вакуума). В результате количество произведенных продуктов сгорания увеличивается наряду с количеством избыточного воздуха и температурой газов.
Расчеты для всасывающих устройств выполняются с использованием фракций номинального объема воздуха.
D VI: количество воздуха, всасываемого в первую поверхность котла.
Определение дополнительного воздуха за i-й поверхностью нагрева равно aI = Si.
Очень важно постоянно контролировать избыток кислорода в газовом тракте для обеспечения идеальных условий сгорания и уменьшения подсоса воздуха в газовом тракте.
Как было указано ранее, коэффициент избытка воздуха определяется путем деления количества воздуха, которое фактически подается, на количество, которое считается необходимым.
, (4)
Где V представляет дополнительный воздух.
Мы можем определить, что объем общего воздуха для горения связан с объемом кислорода без учета снижения содержания азота в дымовых газах, вызванного увеличением количества топлива (его доля незначительна).
. (5)
Количество кислорода, которое не вошло в реакцию, связано с чрезмерным количеством воздуха, которое поставляется для сжигания в виде струи от горелки:
. (6)
Формула азота может быть получена путем замены (5) и (4):
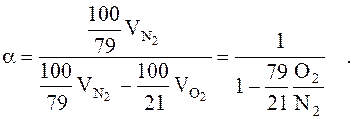
Расчет основан на количестве кислорода, который должен был реагировать при полном окислении горючих элементов, чтобы определить, существует ли химическое подключение.
.
.
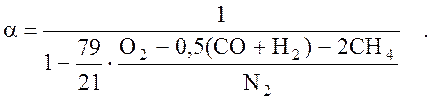
Необходимо выяснить соотношение кислородного, азотного и водородного состава продуктов сгорания для точного расчета коэффициента избытка воздуха.
В действительности, сухая трехатомная смесь в продуктах сгорания и концентрация кислорода – это два более сжатых метода определения соотношения избыточного воздуха.
Основным методом является прямой анализ содержания кислорода. Какие компоненты составляют процентное содержание кислорода в продуктах сгорания?
Убедитесь, что в горючей части топлива нет водорода. Объем диоксида водорода, образующегося в результате окисления углерода и серы, равен объему израсходованного кислорода (C O2=CO2), в то время как концентрация азота всегда остается постоянной.
Формула азота может быть изменена на формулу кислорода при химическом недогорании (CO=0, H2=1):
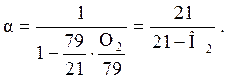
Пусть водород будет единственным компонентом топлива, который может зажечь. Единственными побочными продуктами полного сжигания будут тогда водяной пара, азота и кислорода. Концентрация азота в продуктах сгорания будет на 100%, когда будет превышение воздуха, равного 1. Содержание азота на продуктах сгорания сухого сжигания в результате энергии водорода в топливе.
Содержание кислорода в продуктах сгорания может изменяться в результате изменения концентрации азота. Весь кислород воздуха будет расходиться на окисление водородного топлива при топливном соотношении 4/32 = 1/10 (H2O, 2 N2; 36) для водородного топлива. Концентрация азота в продуктах сгорания всегда будет постоянной и равной 79% при избытке воздуха. Кроме того, формула кислорода дает такие точные значения только при незначительном содержании водорода (например, при сжигании древесины) или при соотношении HR/OU 1/10.
Процентное содержание сухих трехатомных газов используется как основа для второго метода расчета избытка воздуха в продуктах сгорания.
Выглядеть равным ужасному,
где , %.
Соотношение сухих трехатомных газов будет Hg=Oha/8 при полном сгорании топлива в количественных соотношениях (a=1), при условии, что содержание водорода и кислорода соответствует выражению Hg=Oha/8 (весь кислород окисляется топливом воздухом).
.
Hg равен Or/8 в большинстве твердых и жидких топлив. В этом случае оставшийся водород окисляется кислородом воздуха с образованием водяного пара. Все сухие газовые смеси будут содержать оставшееся количество азота, максимум до 21% содержания трехатомного газа.
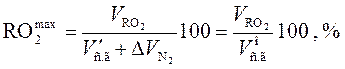
Разница между Hg и Og/8 становится меньше по мере увеличения ее размера.
Топливный коэффициент бунта b – это формула, которая отображает это изменение содержания водорода и кислорода (WT).
.
Следующее предложение можно использовать для выражения максимального количества сухих трехатомных газов в продуктах горения:
.
Основные значения для разных видов топлива, %:
Вещественное топливо. 18 20;
Мазут. 16÷17;
Природный газ. 11÷13.
Объем сухого газа составляет всего 450 мл, если соотношение избыточного воздуха составляет 1 к 10.
Кроме того, содержимое трех воздушных хижин будет меньше, чем:
.
Учитывая, что объем не изменится,
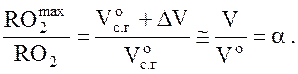
Точность анализа дымовых газов как датчик содержания HO2 и значение RO2 являются основой этого подхода к расчету избыточного воздуха. Применение этого метода к топливу, который содержит карбонаты и издает дополнительный CO2 из -за его минерального состава, представляет проблемы.
Расчеты для избыточного соотношения воздуха с использованием газового анализа
Азотная формула:
(7)
– кислородная формула:
(8)
– по количеству сухих трехатомных газов в продуктах сгорания.
(9)
где
Дата: 2022-07-30;Просмотр: 4580
§
Полнота сгорания топлива в камере и глубина охлаждения продуктов сгорания в топке – два основных фактора, определяющих эффективность использования топлива.
Создавая тепловой баланс, тепло вводится в печь для компенсации тепловых потерь и потерь полезного тепла. Для 1 кг твердого или жидкого топлива или для 10 м3 газообразного топлива рассчитывается тепловой баланс.
Располагаемая теплота
, кДж/кг (м3).
I TL – это физическое тепло, выделяемое при сгорании рабочей массы топлива; IF – это физическая энергия, добавляемая в топку посредством парового дутья или двух пар распыления мазута.
Для большинства сухих твердых топлив с низким содержанием серы p =; аналогично, для газовых топлив p =
Физическое тепло i tl, которое зависит от температуры топлива, поступающего на сжигание, учитывается для твердого топлива с высоким содержанием влаги и жидкого топлива:
iтл = стлtтл ,
Где ttl – температура топлива (прокачка), а stl – удельная теплоемкость топлива, в кДж/(кг).
Температура топлива принимается равной TTL = 20 C летом, а теплоемкость рассчитывается по следующей формуле:
К Дж/(кг С).
Сухая масса топлива имеет следующую теплоемкость:
Бурые угли имеют показатель 1,13 кДж/(кг S).
Каменный уголь имеет значение 1,09 кДж/(кгс).
P A для углей A составляет 0,92 кДж/(KGF).
Физическая жара топлива игнорируется зимой, а DTL = 0 с принимается.
Для обеспечения тонкого распыления в форсунках котельного агрегата температура мазута должна быть достаточно высокой. TTL обычно составляет 90×140 C.
Теплоёмкость мазута, кДж/(кгС).
Пар подается в топку котельного агрегата вместе с нагретым мазутным паром через паровые форсунки, что увеличивает тепловую и энергетическую мощность топлива.
Qф = Gф (iф – 2380), кДж/кг,
Gf – количество пара, расходуемого на нагрев 1 кг мазута; iF – энтальпия воздуха, поступающего в форсунку (в кДж).
P = 0,30,6 МПа, T = 280 ° –350 ° C, а конкретное потребление пара составляет 0,0035 мм/кг масла.
Теплота предварительного нагрева воздуха в нагревателях перед его поступлением во внешний воздухонагреватель равна B. Vn рассчитывается по следующей формуле:
,
Где BV является соотношением объема предварительно нагретого воздуха к объему холодного воздуха на входе воздушного нагревателя, который теоретически требуется;
На 1 кг твердого или жидкого топлива или на 1 м3 газообразного топлива имеющееся тепло p используется для создания полезной и необходимой энергии для производства тепловой энергии.
, (10)
Полезное тепло – полезное тепло (1); потери тепла с выбрасываемыми газами (2); По данным Росстата, потери энергии связаны с понижением температуры атмосферы выше +40 °C и ниже -10 °C по сравнению с 1 градусом Кельвинской климатической зоны, а также с понижением кислорода из-за нагрева газов до 0 °C для 0 °C для 0 °C для охлаждения атмосферы вокруг реакторов мощностью не более 100 МВт/час при поддержании постоянной плотности воздуха в помещениях.
Правая и левая половины формулы (10) делятся на p для получения следующих уравнений теплового баланса:
,
Q1 – это процент полезного тепла, которое было использовано, а k2 – процент тепловых потерь (qu6).
Коэффициент полезного действия котла
.
Большая часть жары, которая была внесена печью и передавалась в рабочее тело. Вода кипит в результате этого тепла, что также приводит к перегреву или испаряется пар. Мощность, используемая для нагрева воздуха. Теплая вода способствует тепловым потерям.
Общая теплоемкость котла
Бойлер для нагрева воды необходим для водогрейного котла.
, кВт,
D IN – это скорость потока воды через котел (в килограммах в секунду), а KJ – энтальпия жидкости на входе и выходе.
– для парового котла
, кВт,
Где DPE – расход перегретого пара, кг/с; DPR – расход продувочной воды, КДж; IPF – энтальпия питательной воды; и IKIP – расход перегретого пара.
Самые значительные потери тепла в котельной установке обычно происходят с дымовыми газами:
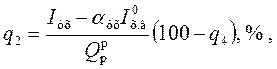
Который и, как следствие, энтальпия газов, покидающих тело; теоретический объем холодного воздуха.
Газообразные горючие компоненты Co, H2 и CH4 могут присутствовать в продуктах сжигания топлива в результате химического подключения;Тем не менее, из -за низких температур в камере сгорания, послеочивления по существу невозможно.
Следующие факторы могут привести к химической неполноте сжигания топлива:
· общего (или местного) недостатка воздуха (αт);
Недостаточное перемешивание (конструкция горелки, процесс сгорания топлива);
Выявление высоких или низких значений нагреваемого напряжения печи (в первом случае, низкая температура печи; во втором уменьшение времени пребывания в салоне газа и невозможность завершения реакции Gorenje).
Тип топлива, процесс сгорания и аэродинамика камеры сгорания влияют на то, сколько тепла теряется из -за химического подключения.
Общая теплота неполного сгорания горючей массы определяет потери тепла с химическим недожогом:
100, % ,
Объемные концентрации не полностью сгоревших топливных продуктов, CO, CH4 и H2, в сухих продуктах сгорания; Vcr, объем сухих продуктов сгорания (м3\/кг);
Потери тепла при химическом недожоге снижаются до коэффициента избытка воздуха (рис. 2) и загрузки печи
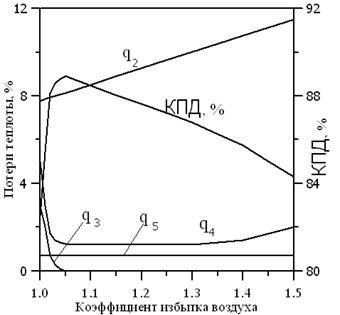
Рис. 2. Как рассчитать зависимость между эффективностью и тепловыми потерями
Влияние коэффициента избытка воздуха на кондиционирование
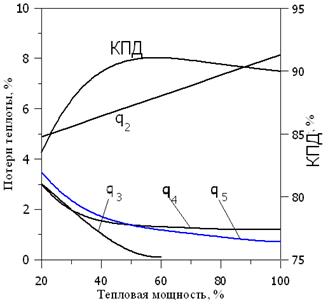
Рис. 3. Зависимость от КПД и теплопотерь
Сколько определяется термической способностью котла
Химический недожог при a = 1 вызван недостаточной аэродинамикой современных горелок и камер сгорания, которые теоретически обеспечивают идеальное смешивание топлива и воздуха. Химического недожога нет, если коэффициент избытка воздуха acr (кривая q3) меньше 2. Обычно acr колеблется от 1,02 до 1,03.
При сжигании твердого топлива (торф, уголь) частицы кока-колы, полученные из известняков, механически недолговечны, потому что они находятся в зоне высокой температуры. При сжигании газов и мазута в зоне высокотемпературных без доступа к воздуху может произойти механическая короткая. Потери от механических коротких сжиганий составляют Q4 = 0,5-5% в типичных условиях эксплуатации. Потери от сжигания газа и мазута минимальны (обычно менее 1%).
Потери тепла в камере сгорания при камерном сжигании твердого топлива делятся на потери со шлаком и унос, при этом потери тепла со шлаком составляют большую часть тепловых потерь.
Коэффициент избытка воздуха влияет на потери q4. Развитие зон недостатка кислорода и неполное смешивание топлива и воздуха на выходе из горелки вызвано избытком воздуха ниже оптимального недожога.
Температура в зоне сгорания падает в A> Aont, а реакции окисления замедляются. Из-за увеличения объема продуктов сгорания время пребывания частиц в высокотемпературной зоне также уменьшается одновременно.
Раннее воспламенение частиц кокса и длительное горение в кинетической области являются причинами повышенной потери q4 в топливе с низкой реакцией.
Для расчета потерь тепла, связанных с механическим неполным сгоранием, используется следующая формула:
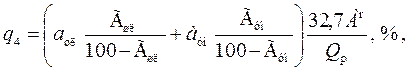
G SHL и оружие стоят за процент горючих частиц в шлаковых отходах (GSHL или Hunn), соответственно, и оружие для процента пепла в шлаке.
0,2-2,5% тепла от внешнего охлаждения Q5 теряется в окружающую среду
Следующая формула рассчитывает потери тепла, связанные с физической энергией шлака:
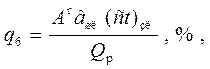
Где измеряются температура и теплоемкость шлака.
Температура дымовых газов немного снижается при уменьшении тепловой нагрузки котла, что уменьшает потери тепла от дымовых газов. При уменьшении скорости смешивания топлива и воздуха потери тепла из-за химического и механического недожога увеличиваются. Поскольку абсолютная величина этих потерь остается постоянной при снижении нагрузки на корпус, удельные потери тепла через кладку увеличиваются. Аналогично этому, КПД котлоагрегата достигает максимальных значений при снижении нагрузки (см. рис. 3). ).
Баланс между доступным и полезным теплом может быть использован для оценки расхода топлива В при его подаче в топочную камеру котлоагрегата:
, кг/с или м3/с.
Расчеты расхода топлива с учетом механически неполного сгорания топлива
, кг/с.
По прямому балансу:
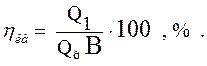
Дата: 2022-07-30;Просмотр: 1518
§
Основной компонент сгорания образуется кусками топлива во время сгорания в плотном слое (рис. 5). Сплошное топливо загружается в слое определенной толщины на распределительную решетку для зажигания, а воздух взорван снизу вверх или сверху вниз – воздух поднимается от земли до потолка. Как частицы из тонкого сгорания, так и летучие соединения (H2, CO), высвобождающиеся из слоя топлива во время его нагреваемого ожога над ним. Предел стабильности постельных принадлежностей устанавливает ограничение на скорость потока газового воздуха. Помимо определенной точки, скорость воздуха (и впоследствии дымоходу) увеличивается увеличение уровня, вызывает увеличение слоя. Это приводит к удалению многих меньших частиц топлива из печи и снижает потерю тепла, потому что полидисперсное топливо всегда загружается в кровать.
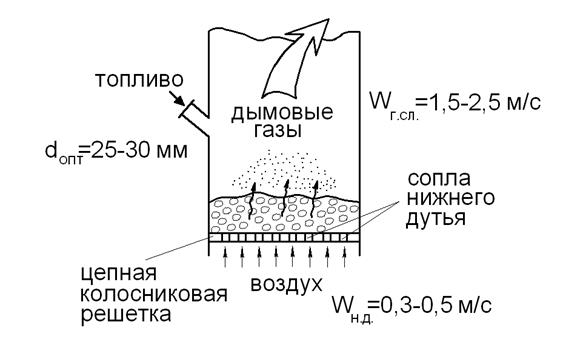
Рис. 5. В плотной среде.
В области постельного белья, где воздушный кислород почти полностью потребляется (рис. 6), его высота составляет два -три диаметра топлива, или KCIS = (2,4) к.
Зона восстановления (за которой происходит восстановление CO2 и H2) присутствует на поверхности частиц углерода, если высота слоя больше высоты зоны кислорода (C = 2O – CO H2 ).
Дымовые газы включают горючие газы, а также CO2, H2O или N2.
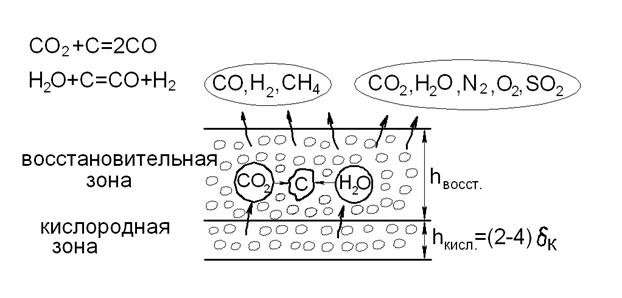
Рис 6. Топливный слой
Высота слоя в слоевых топках должна соответствовать высоте кислородной зоны. Дополнительный воздух подается над слоем топлива в объеме топки после удаления из слоя угольной пыли и продуктов неполного сгорания (H2, CO).
В зависимости от того, как топливо подается в колосниковую решетку и перемещается по ней, топочные устройства, используемые для послойного сжигания, делятся на различные категории. Шурка слоя необходима для удаления шлака и сжигания агломерата (при использовании угля gorenje). Уголь и каменный уголь, используемые в качестве компонента котла, сжигаются в немеханизированных топках, где все операции выполняются вручную.
Промышленное отопление все чаще использует слоистые печи с пневмомеханическими чашками и решеткой о возврате цепи (рис. 7).
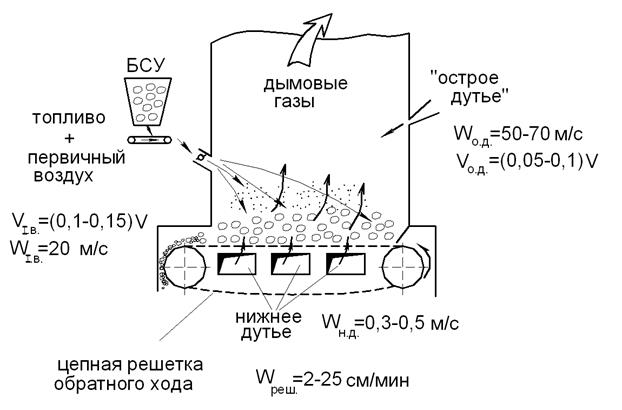
Рис. 7. Печь обратного потока, которая является полумеханической
Топливо непрерывно перемещается со скоростью от 2 до 25 см/мин от необработанного угля у кормления ремня к лезвиям ротора пневмомеханического скребка, а затем к печи через решетку. Кровать решетки состоит из различных компонентов решетки, которые прикреплены к бесконечной серии шарнирных цепочек. Специальные форсунки используются для доставки воздуха сгорания. Большие части падают на спину и проводят там больше времени на решетку из -за законов инерции. Специальный воздух печи, который составляет 10% от общей скорости потока и питается со скоростью 20 м/с, зажигает наименьшие частицы (частицы с диаметром менее 1 мм) на месте.
Через сопла, встроенные в заднюю стенку печи, воздух также подается в объем печи со скоростью 50 м/с (5-10% от общего расхода). Летучая зола из золоуловителя обычно возвращается в топку резким ударом. Q4 может достигать 10%.
Учитывая, что часть топлива сгорает в пламени, описанная топка является факельной.
Для слоевых топок куски угля должны быть размером 2500 на 50 мм. Для слоя в целом скорость нижнего дутья, wnd=1-1 = 0,32 м/с, соответствует оптимальной скорости газов, выходящих из слоя (с точки зрения устойчивости слоя), Wr=1,502,5 м/с.
В чем преимущества двухслойных топок?
Достаточная простота эксплуатации;
Отсутствие систем подготовки пыли для измельчения угля;
Устойчивой работы при различных нагрузках.
Слоевое сжигание имеет ряд недостатков, в том числе:
Ограниченная производительность, включено время
Низкий КПД обусловлен более высокими потерями тепла от механического недожога и дымовых газов (из-за требования поддерживать высокий коэффициент избытка воздуха в 1,4 раза).
сжигать только твёрдое топливо;
Сжигание топлива с очень высокой зольностью и влажностью проблематично (невозможно).
Дата: 2022-07-25;Просмотр 11301
§
Идея факельных (камерных) печей заключается в том, что топливо продувается через горелки вместе с воздухом, необходимым для горения.
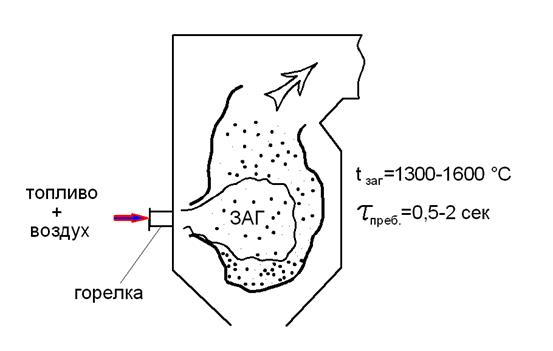
Рис. 8 – Факельный метод
Поток воздуха и побочных продуктов сгорания непрерывно переносит топливо. Перед выходом, во время процесса горения, ведущего к входу (выходу из горелки), топливо сгорает, образуя факел, заполняющий объем камеры сгорания. Температура в зоне активного горения колеблется от 1300 до 1500 С, а время, которое частицы топлива проводят там, составляет от 0,5 до 2 секунд. Для обеспечения полного выгорания топливо перед поступлением в топку предварительно просушивается и тщательно растапливается, а жидкость в течение этого короткого периода распыляется форсунками (для газовых турбин).
Размольные устройства измельчают твердое топливо, которое затем продувается через пылевые горелки (рис. 9). Из-за широкого диапазона изменения тепловых свойств угля конструкции горелок невероятно разнообразны. Выход летучих, который в значительной степени определяет реакционную способность и реакцию сланца, может колебаться от до 2% для метаантрацита до до 90% для эстонского сланца, в зависимости от типа топлива. В большинстве пылеугольных горелок первичный воздух смешивается с топливом до его поступления в топку, а оставшийся воздух смешивается со смесью уже после прохождения пламени. Первичный воздух используется для сушки и транспортировки угольной пыли к заслонке.
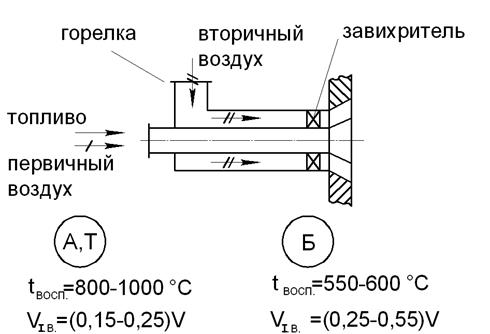
RIS 9. Райный достойный паннеров
При нагревании и термическом разложении угольной пыли в камере сгорания выделяются летучие вещества, так как образуются гомогенные смеси. Количество первичного воздуха VIB (доля от общего объема воздуха) определяется выходом отработанного газа, так как он должен обеспечить сгорание летучих веществ. Доля первичного воздуха VIB составляет 0,15’1:25 для углей с низким выходом летучих (таких как антрацит и тощий уголь), температура воспламенения которых колеблется от 800 до 1000 C.
В этом случае угольная пыль уже смешивается с некоторым воздухом во время сжигания (вторичный воздух), который поставляется в печь через специальный канал.
Кислород первичного воздуха расходуется в основном в процессе сгорания летучих веществ. Нагрев и воспламенение частиц кокса ускоряются за счет сгорания летучих веществ. Кислород во вторичном воздухе является основной причиной горения частиц кокса.
Теоретически сжигание угольной пыли представляет собой более простую систему. Однако в реальных условиях происходит сжигание полидисперсных частиц, и только для каждой отдельной частицы (или всей фракции) фазы выделения летучих веществ и сжигания коксового остатка протекают последовательно. Эти процессы происходят одновременно для всей факельной массы, включая все составляющие ее частицы. Для бурых углей и торфа максимальный размер частиц при факельном сжигании составляет несколько миллиметров, а для других материалов – несколько сотен микрометров.
6.2.1 В каком положении должны находиться горелки относительно стенок топочной камеры?
В то же время факторы, отличные от дизайна горелки или параметров режима печи, влияют на то, как возникают интенсивные процессы сжигания, тепло и массовый обмен. Переднее расположение горелки чаще всего используется для обычных однокамерных печей (рис. 10).
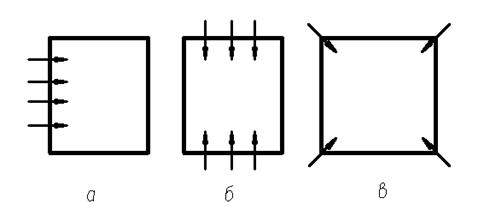
Рис. 10. Схемы расположения топочной камеры
Фронтальный, B, приближающийся из угла
Фронтальное расположение горелок (рис. 10а) – это место, где струи от различных видов пламени объединяются в один непрерывный поток. Расширяясь, струя втягивает (выбрасывает) топочные газы, снижая при этом количество окислителя в воздухе. Рекомендуется использовать вихревые горелки, которые дают относительно короткий факел, в качестве противоположного источника тепла, чтобы струя не касалась противоположной стенки топочной камеры во фронтальном положении.
Горелки устанавливаются спереди и сзади или на противоположных боковых стенках при встречном расположении (рис. 10б), хотя возможно как фронтальное расположение, так и встречная комбинация.
На рис. 11 сравнивается пламя нециркулирующего параллельного потока с моделями свободно распространяющегося пламени закрученной осесимметричной горелки при различных углах закручивания вторичного воздуха.
В печи с противолежащим расположением происходит обдув концентрированной струей, и от нее расходятся два направления. Когда импульсы равны, ток может течь в потоках асимметрично, и горелка окажется на одной из стенок.
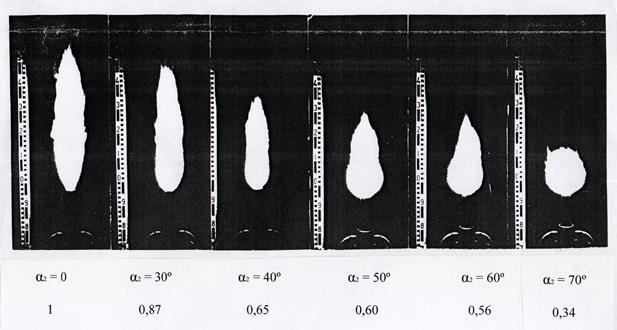
Рис.11. длинна факела вихревой горелки Lвихр
Вторичный воздух закручивается под различными углами 2
В отличие от прямой Flare LPR
При встречном смещении горелок потоки взаимно проникают друг в друга, улучшая заполнение пламенем объема топки и уравновешивая температурное поле.
В зависимости от угла расположения горелок (рис. 12) они могут быть расположены следующим образом: диагонально, блочно, тангенциально и традиционно. Эти варианты расположения, как и встречное смещение, имеют ряд преимуществ.
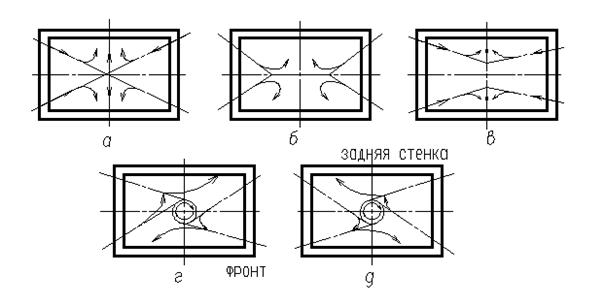
Рис.12. Схема установки горелок
Блок и линия наклона существуют в диагональных плоскостях, а d, g – касательные.
Дальнейшая турбулизация (закрутка) потока с помощью вихревых горелок интенсифицирует процессы тепло- и массопереноса, однако, если импульсы не совпадают, аэродинамика результирующего потока может исказиться.
Профиль скорости, скорость вдоль оси струи и способность струй выбрасывать материал резко изменяются в вихревых горелках (рис. 13).
Статическое давление падает при небольшом повороте оси струи. Центробежные силы, возникающие при движении вращающихся частиц потока, приводят струю в движение. Если равновесие сохраняется, то движение свободной, не закрученной струи можно использовать для представления профиля осевой составляющей скорости (рис. 13).
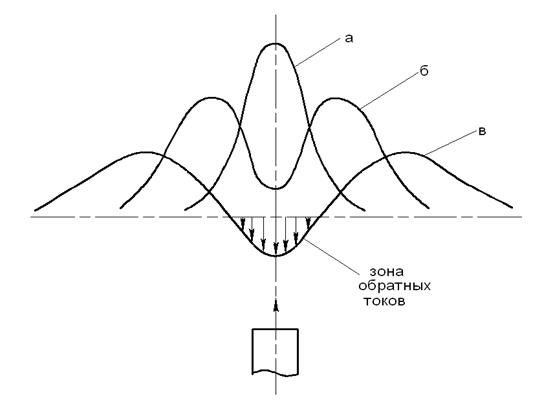
Рис. 13. Осевая составляющая профиля скорости изменяется.
По соседству появились новые общины.
Слабо закрученная струя; сверхкритическая закрутка) сильная закрученная струя
Когда поток более скручен, силы сжатия уравновешивают часть осевого импульса и замедляют поток вниз. Наибольшее осевое торможение также происходит в присутствии этой оси, если падение давления происходит на его оси. Профиль поворота с депрессией в середине создается с дальнейшим увеличением скорости (рис. 13, кривая B).
Последующее увеличение количества салфеток приведет к тому, что силы сжатия превысят осевой импульс потока вблизи оси и заставят поток повернуть вспять (рис.). 13).
Ключевым компонентом в поддержании пылевидного пламени является обратный вихрь, создаваемый по периметру горелки.
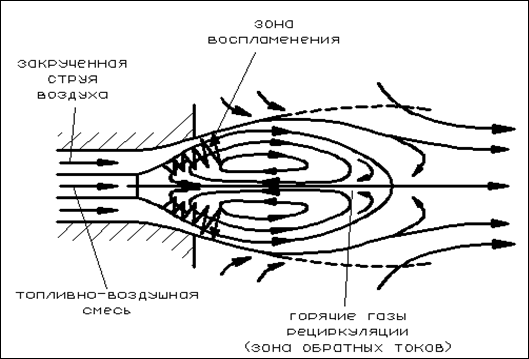
Рис.14. Зона реверсивных течений в выходе вихревой горелки
Вторичный воздух закручивается с помощью осевых или радиально расположенных направляющих лопаток, в то время как угольная пыль равномерно воспламеняется вихревыми горелками (рис. 27). Из-за этого поток, поступающий в пространство печи, в конечном итоге образует сильную, турбулентную, закрученную горелку, на которой создается вакуум. Размер внутренней зоны рециркуляции (зоны пониженных токов) и ее удаление от среза горелки определяются геометрией пламени. Это ускоряет нагрев топливной смеси с первичным воздухом и ее воспламенение, стабилизируя факел в процессе.
В каждой топке хранится незначительное количество угля – не более нескольких десятков килограммов. Это позволяет более точно контролировать расход топлива и воздуха (по сравнению со слоевым сжиганием), если когда-нибудь возникнет необходимость изменить тепловые характеристики печи. Факельный способ сжигания требует высоконадежной непрерывной подачи угольной пыли в топку, что связано со значительным риском взрыва при возобновлении подачи топлива. Горелки часто присутствуют в пылеугольных котлах.
Основные преимущества стратифицированного сгорания по сравнению с вспышением
Во время процесса обогащения камерные печи могут сжигать любое топливо, включая уходы отходов;
Возможность построить печь любой желаемой мощности;
Даже если сжигание угольной пыли не приводит к увеличению тепловых потерь, при низких коэффициентах избытка воздуха производительность достаточная;
повышенный мехнедожог.
К недостаткам следует отнести следующее:
Предел более низкой пропускной способности ограничен (тепловая выработка от горящей угольной пыли не может быть менее 20 МВт), то есть уголь не может быть сожжен в небольших печи;
Увеличение потребления энергии на личные нужды в результате необходимости использования системы пылеприготовления (СПП) для подготовки топлива;
Оксиды азота и серы, два токсичных газа, присутствуют в воздухе в более высоких концентрациях.
Дата: 2022-07-25;Посмотреть 2843
§
Пылевидное угольное пламя может устойчиво гореть при высоких температурах в активной зоне факела. Этот температурный диапазон вызывает значительное увеличение скорости образования оксидов азота “теплового воздуха” (мы обсудим эти химические соединения в разделе 11).
Na = это.(11).
Предельно допустимая концентрация (ПДК) высокотоксичного диоксина Н2, который образуется при диоксидировании оксида азота в атмосфере, не должна превышать 0,085 мг/м3 в приземном слое. Даже строительство высоких дымовых труб (для распространения газов на большую площадь) не всегда гарантирует экологическую безопасность, особенно в местах скопления большого количества топлива.
Сжигание серосодержащего (фосфор-содержащего) топлива приводит к выработке кислотно-дождя и токсичного оксида азота.
Температура в зоне активного горения должна быть снижена до 850-900 С для уменьшения вредных выбросов, так как при этой температуре диоксид серы соединяется в растворе со структурами кальция и магния (MgO реагирует аналогично) и скорость образования оксида азота по реакции (11) низка.
SO2 CaO 0,5O2 = CaSO4 . (12)
Кристаллы карбоната натрия добавляются в топливо, если содержание оксида кальция и магния в золе недостаточно, чтобы связывать весь CACO3 (как правило, вам нужно в два или три раза его количество). Известняк быстро разлагается на CAO, CO2 и Gypsum SSO4 в 900 ° С.
С другой стороны, значительное количество горючих органических отходов образуется в результате деятельности человека. Согласно общепринятому определению, следующие предметы не могут считаться топливом (они им не являются): “хвосты” обогащения угля и отвалы, образующиеся при добыче угля; многочисленные отходы, образующиеся в целлюлозно-бумажной или лесной промышленности – шлак угля из шахтных стволов с высокой концентрацией минеральных компонентов на поверхности почвы соответствующего слоя породы или их соединений с щелочными компонентами). В слоях зола блокирует доступ кислорода к горючим частицам или забивает воздушные сопла; в камерах она затрудняет работу двигателя.
Создание топочных устройств для сжигания таких материалов становится все более актуальным в результате необходимости снижения вредных выбросов и развития безотходных технологий. Метод сжигания в кипящем бульоне был создан именно по этой причине.
Слой тонкодисперсного материала, который был взорван вверх потоком газа со скоростью, превышающей пределы устойчивости плотных слоев, но недостаточной для выноса частиц из слоя, называют кипящим (псевдоожиженным). Сам слой приобретает определенные характеристики и поведение, создавая впечатление кипящей жидкости из-за интенсивной циркуляции частиц в ограниченном объеме.
Когда топливо непрерывно поставляется, на сетке будет содержатся фиксированный сжигательный слой, если в камере сгорания установлена сетка (рис. 15а), на которую расположен слой угля, а воздух поставляется в сетку в сетку. Нагрейте слой выпуском газообразных продуктов сгорания.
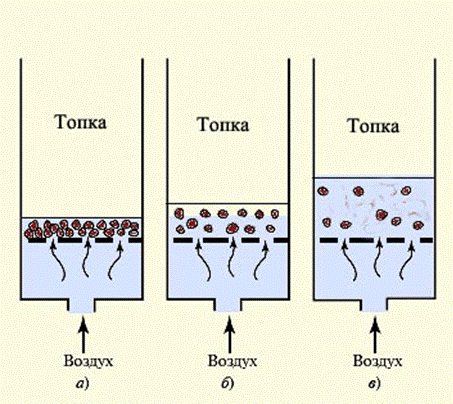
Рис. 15.Модификация топливного слоя
Различные скорости взрыва при более низких скоростях
Частицы топлива в решетке будут испытывать скоростное давление, если увеличить подачу воздуха снизу. Толщина топливных элементов будет увеличиваться по мере их взвешивания в атмосфере (рис. 15а). Процесс начинается, когда сжижающий агент движется со скоростью, вдвое превышающей скорость его потока P (рис. 16). Первая критическая скорость (Wcr1) – это наименьшая скорость, при которой происходит псевдоожижение.
Толщина слоя еще больше увеличивается с ростом скорости. Создается впечатление, что слой топлива “кипит”. Стационарный кипящий слой с пузырьками – вот как называется этот слой (рис. 15в, 16).
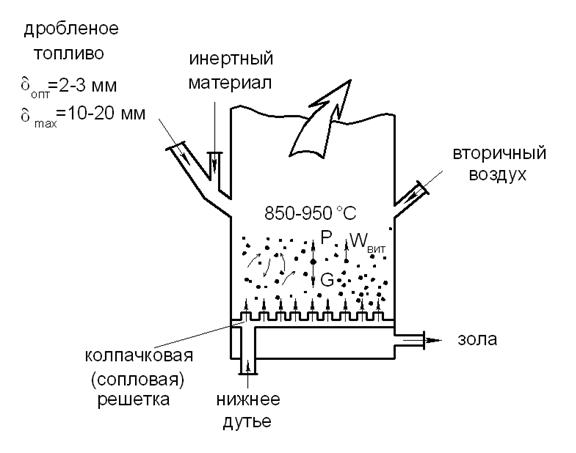
Рис. 16.Стативный кипящий слой (SCS)
При достижении состояния P G частицы остатков топлива начинают выноситься из слоя, поскольку подъемная сила, действующая на частицы топлива, сильно возрастает при более высоких скоростях воздуха (потому что они не успевают сгореть).
Вторая критическая скорость, или Wcr2, – это точка, в которой аэродинамический момент равен гравитационному притяжению частиц топлива.
Настоящие жидкостные устройства печи работают между WKR1 и WKR2 в секунду.
Когда скорость в кипящем слое близка к Wkr2, становится очевидным различие между печью со стационарным кипящим слоем и печью с циркулирующим горячим слоем. Поскольку слой состоит из полифракционных инертных частиц с различной плотностью, обе критические скорости в этом случае могут быть точно определены только для монодисперсного материала с постоянной плотностью.
В печи с кипящим слоем горючий материал обычно редк, и когда он присутствует, обычно это топливный пепел (при сжигании углей с высоким содержанием). Увеличение тепла и массопереноса в слое вызвано интенсивным смешиванием твердых частиц под воздействием разжигающего воздуха. Вы можете сохранить температуру, когда нет шлака слоя, погрузившись в кипящий слой.
В стационарной печи с псевдоожиженным слоем (см. Рис. 1, 16) известняк или песок с гранулированным пеплом или другим гранулированным материалом, образующим в смеси, измельченный уголь – от 1,5 до 2 мм на 1 м3 под действием восходящего воздушного потока через решетки крышки вВторая часть печи, а также другие материалы из кишечника угля: торфяного шлака для обжаривания не приправленных дров/подвесного топлива “Sputnik” при температуре примерно 450 градусов по Цельсию.
Добавляя несколько тонко диспергированных материалов (в соотношении около 1: 1) вместе с топливом, можно сохранить температуру псевдоожиженного слоя в течение необходимых диапазонов и контролировать процесс «кипячения».
Слои и самая простая псевдоожиженная печь имеют много структурных компонентов. Это основное различие. Высота и поперечное сечение жидкости поддерживаются при постоянной температуре из -за смешивания частиц, обеспечивая высокую теплопередачу на поверхности теплообмена.
С помощью технологии псевдоожиженного слоя можно сжигать дробленое топливо со средним оптимальным размером частиц до 10-20 мм (или до 35 мм в случае отжима древесных отходов). По сравнению с обычным топливом на углекислотных заводах США или Японии, такой размер частиц соответствует рабочей максимальной скорости кипящего слоя 1,5-2 м/с, что почти в два раза превышает предельную скорость устойчивости плотного слоя, состоящего из таких осколков диаметром 1 км и более. Их количество должно составлять не менее 5-7% от общего объема горючего газа.
Циркулирующие печи – это технология сгорания с жидкости второго поколения (рис. 17).
Основное различие состоит в том, что все несгоревшие частицы образуют циклон за печью и перемещаются обратно. Частицы и циклоны остаются в закрытой системе печи, пока они не будут сожжены. Эти реакторы сохраняют все экологические преимущества, будучи почти такими же рентабельными, как камерные печи.
Циркулирующие псевдоожиженные печи обеспечивают эксплуатацию без чрезмерного воздуха и имеют более высокую степень выгорания топлива (около 90% против 70-85%).
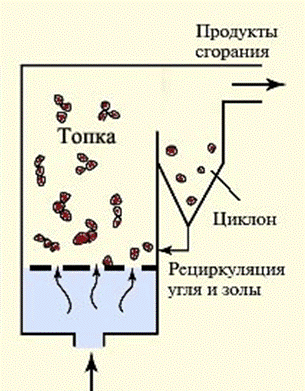
Копать землю.17. Написание (CCS)
Каковы преимущества печей с кипящим слоем перед печами со стационарными пылеулавливающими лентами?
Меньший коэффициент конвективного теплообмена;
Удаление излишнего избыточного топлива и производственных отходов стало возможным благодаря длительному присутствию частиц в слое;
Возможность спроектировать топочное устройство меньшего размера, не требующее системы пылеудаления;
Известняк, добавленный к слою, связывает серу от топлива с остатком золы, снижая выбросы серы антриудки;
Отсутствие термических оксидов азота обеспечивается низкой температурой слоя (800,950°C), что снижает количество газов, выбрасываемых в атмосферу.
Однако, несмотря на свои преимущества, низкотемпературные котлы с кипящим слоем, работающие на топочном топливе, имеют и серьезные недостатки:
Из-за ограниченного диапазона рабочих температур реактора с псевдоожиженным слоем трудно регулировать мощность котла.
Не рекомендуется прекращать горение, если температура слоя падает ниже 750С;
) истирание частиц твердых отходов, увлекаемых потоком оживляющего агента;
эрозия поверхностей нагрева;
Ограниченный диапазон скорости для разжижающего агента;
Вентиляторы высокого давления, которые подают воздух в зону горения и создают псевдоожиженный слой, требуют больше энергии для работы.
Котлы с кипящим слоем могут быть использованы для работы на модернизируемых ТЭС в зависимости от необходимости. В настоящее время в мире эксплуатируется более 200 энергоблоков, оснащенных котлами с кипящим слоем. Для измельчения каменного угля различных месторождений в России разрабатываются паровые котлы производительностью 160, 500 и 1000 т/ч.
Другое использование печи с псевдоожиженными слоями за пределами энергетического сектора включают:
Сжигание колчеданов с целью получения СО2;
Жареные металлы и их концентраты;
Термическая нейтрализация вредных веществ, включая осветление осадка сточных вод и бытовых отходов, в твердой, жидкой и газообразной форме
Дата: 2022-07-30;Просмотр – 2277
§
6.4.1 Ворт при высокой температуре сгорел
В циклоне-вишенке присутствует T BV (рис. 18). С помощью этой техники можно сжигать газообразное, жидкое и измельченное твердое топливо (с частицами размером до 5 мм).
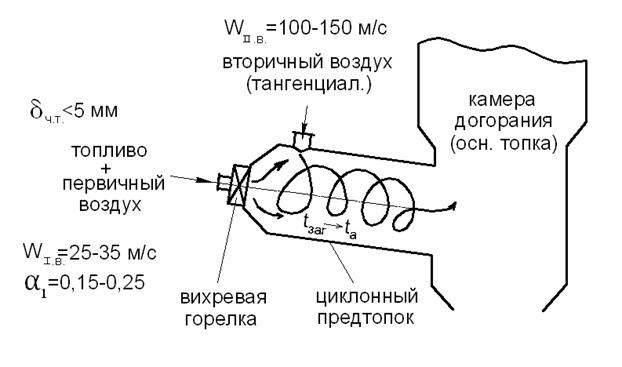
Рис.18. Высокотемпературное вихревое сжигание
Перед основной топкой (камерой горения) устанавливается циклонум. Вдоль оси прогнозирования подается топливо и первичный воздух, а вторичный воздух направляется со скоростью около 100 м/с в развивающийся циклон. Можно сжигать более крупные частицы топлива, чем при факельном способе сжигания (при температуре 200-300 градусов Цельсия), так как большое количество частиц топлива врывается в вихревой поток, продлевая время их пребывания на поверхности при температуре до 2000 градусов Цельсия.
Основной верхний объем имеет циклонно-оральные камеры, в которых осуществляется ступенчатый спуск. В прогнозе наблюдается высокая турбулентность и сильная центробежная сила, сопровождающая циклона-ральное движение среды.
Эта техника очень редко применяется в энергетическом секторе. В основном это реакторы с кипящим слоем, которые используются в технологических процессах и т.д.
6.4.2
Низкотемпературный (НТВ) способ горения был создан профессором В. А. Померанцевым (19) в качестве альтернативы вихревому горению.
Основа технологий N TV-это идея грубого твердого топлива сжигается при высоких температурах в условиях множественной циркуляции частиц.
N TV-Top имеет две зоны сгорания: прямое потоки и вихрь, которые расположены по высоте. От устья трубчатой воронки до горелок вихревая зона заполняет нижнюю часть печи. В верхней части печи площадь сгорания прямого потока расположена над вихревой зоной.
Взаимодействие двух организованных потоков создает аэродинамику вихревой зоны: первый образуется топливно-воздушной смесью, поступающей в топку через горелки, а второй – горячим воздухом. В нижней части топки создается вихревое движение, когда потоки движутся навстречу друг другу и объединяются, образуя пару сил.
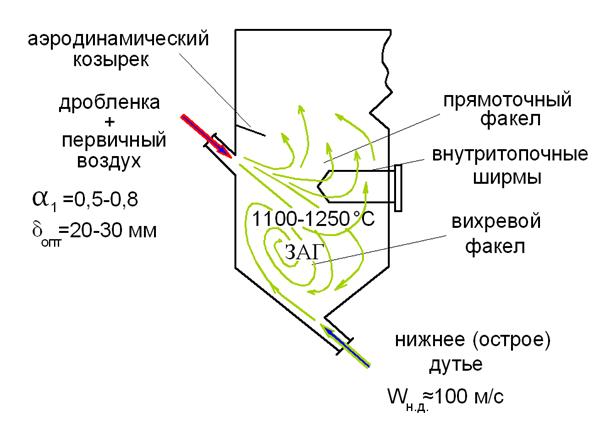
Рис.19. Низкотемпературная вихревая топка Померанцевой
В отличие от традиционной технологии полосагога, которая ставит большую часть топлива (до 95%) в так называемую «зону активного сгорания» рядом с горелками и занимает относительно небольшой объем камеры печи, этот метод распределяетТопливо по всей камере печи. В результате максимальная температура вихревой печи (примерно 100 ОС) падает, и, благодаря активной аэродинамике, уровень температуры выровнен. Из названия очевидно, что вихрь низкотемпературный.
Установка внутриклетной ширины нагрева позволяет уменьшить размер камеры печи из-за снижения температуры, коэффициента конвекции и увеличения конвекции поверхности котла.
Низкая температура в зоне активного горения и бесступенчатая подача окислителя к топливу являются характеристиками NOx-топки. Температура продуктов сгорания в традиционной топке не поднимается выше 1100 оС. Воздушная зона печи изотермична; вихревой зоны нет и быть не может; при таких температурах количество образующихся воздушных (воздушных) оксидов углерода минимально. Коэффициент избытка воздуха (доля первичного воздуха) в горелках составляет от 1,0 до 0,5 в зависимости от марки топлива. По сравнению с традиционной технологией сжигания NOTW концентрация азота снижается на 20%.
Создаются благоприятные условия для связывания оксида серы в НТВ-топе. На активное связывание оксидов серы с основными кислотами (CAO, MG) влияет низкая температура. Помимо меньшего плавления (т.е. большой поверхности реакции) частиц золы и большей площади частицы пыли на частице золы при движении вдоль поверхности потока, этому процессу способствует увеличение времени, которое связывающие компоненты проводят в вихревой зоне. В зависимости от марки топлива, НТВ-технология сжигания позволяет увеличить содержание оксидов серной кислоты в газовом тракте котла на 20-50%. Оксиды железа могут быть более эффективно связаны в вихрях при использовании сорбентов на основе SAO.
Большее количество летучей золы образуется в результате повышенного помола топлива при сжигании HTS. Испытания золоуловителей, модифицированных для сжигания HFO, показали улучшение эффективности электрофильтра.
Улучшенные показатели вихревых печей по вредным выбросам обеспечиваются за счет более низких температурных режимов, ступенчатых окислителей и многократной циркуляции частиц горящего топлива (GTB).
Высокая устойчивость к воспламенению топлива – это особенность -горелки, которая особенно важна при сжигании низкосортного топлива. Несмотря на пониженную температуру, в вихревой зоне печи создается устойчивый механизм благодаря запланированной многократной циркуляции частиц горящего коксового топлива и поэтапному отводу подводного воздуха. Значительную роль в этом играет конструкция горелочно-сопловых устройств и аэродинамические приемы, обеспечивающие взаимодействие пламени и воздуха. Эффективное сжигание низкосортного топлива без подсветки пламени пылью возможно с помощью горелки.
Полностью устраняя наслоение на поверхностях нагрева котла, N TV-розжиг повышает эксплуатационную надежность котла. Количество расплавленных частиц золы в зоне активного горения уменьшается из-за более низкой температуры, что снижает вероятность образования отложений на поверхностях нагрева котла.
Компания N TV создала технологию, которая позволяет сжигать твердое топливо на различных материалах, включая торф и бурый уголь.
Следующие диапазоны соответствуют характеристикам, оцениваемым во время сжигания NTV твердого органического топлива:
| · влажность на рабочую массу, Wrt , % | 14÷75; |
| · зольность на рабочую массу, Ar , % | 5÷50; |
| · выход летучих на горючую массу, Vdaf, % | 23÷90; |
| · теплота сгорания, Qri, МДж/кг | 4,2÷26; |
| · содержание серы на рабочую массу, Sr, % | 0,2÷3,0; |
| · содержание азота на рабочую массу, Nr, % | 0,4÷2,0. |
Н ТВ-сжигание
Н ТВ-технология позволяет:
- Упростить систему подготовки топлива (возможность сжигать дробленый уголь с размером частиц до 20÷30 мм), повысить ее эффективность, обеспечить взрывобезопасность, снизить затраты на подготовку топлива к сжиганию, увеличить срок службы посевного оборудования;
- Стабилизировать зажигание и горение, избегая “вспышки” при использовании газа или мазута, даже при сжигании низкосортного топлива;
- Обеспечить стабильный процесс горения независимо от изменения нагрузки котла и технических характеристик топлива, унифицируя топку в топливе
По умолчанию:
Увеличение количества механических ожогов в результате присутствия крупных, незамеченных частиц;
эрозия внутритопочных поверхностей нагрева.
Когда потоки топлива и воздуха поставляются в камеру печи через прямые горелки или вихревые горелки (а иногда и через рециркуляционные газы) в промышленной отрасли тепловой энергетики, происходит основное сжигание. Есть моменты при использовании кипящих слоев, низкотемпературных вихрей и циклонов.
Дата: 2022-07-30;Вид: 1854
§
Количество вещества, прореагировавшего в единицу времени, в химической кинетике определяет скорость гомогенной реакции:
, кмоль/(м3’c).
В закрытой системе при V = const .
Здесь знак минус означает падение концентрации вещества в ходе реакции.
Молекулы должны столкнуться с действиями. Их интенсивность увеличивается с количеством столкновений.
Скорость окончательных подметок или XapkHeTepked thements веществ ISXOD может использоваться для описания поездки.
Из скорости потока примера 2H2O = 82O4 видно, что его значение превышает кислород в единицах времени. В результате скорость реакции не соответствует скорости потока водорода. Необходимо указать начальную составляющую (начальную или конечную) скорости реакции, чтобы избежать этой двусмысленности.
Обратимая реакция, как правило, не вредна.
aA bB ↔ dD fF
При постоянной температуре отношение остается неизменным:
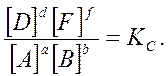
Закон действующих масс, который описывает эту взаимосвязь, выражается следующим образом:
Отношение полученных равновесий продуктов реакции к сумме их коэффициентов постоянно при постоянной температуре.
Константа равновесия конкретной реакции является постоянной CW. Константа рассчитывали с использованием концентраций, как указано индексом «c».
Равновесие смещается в сторону продуктов прямой реакции, если константа равновесия высока. Реакция называется «практически необратимой», если константа равновесия большая, и как «почти без реакции», если она маленькая. Только при постоянной температуре постоянная равновесие для каждой обратимой реакции имеет постоянное значение. При различных температурах постоянная равновесия приобретает разные значения.
Скорость химической реакции увеличивается пропорционально со временем в закрытой однородной системе, работающей при постоянной температуре.
Продукты Реакции
Концентрация реактантов в любой момент времени пропорциональна сумме их индивидуальных взносов.
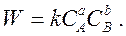
Кроме того, накопление продуктов реакции может быть направлено на противоположный процесс.
Таким образом, для реакции горения водорода необходима энергия пара.
2Н2 О2 = 2Н2О,
Закон действующих масс утверждает, что скорости прямой и обратной реакции:
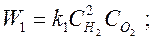
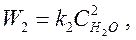
Коэффициенты пропорциональности скорости реакции – K1 и 2.
Количество молекул, которые фактически сталкиваются и вызывают реакцию, определяет константа скорости реакции.
Последняя скорость реакции дается WHZ = W1 – W2. При W1 = W2 вы не можете рассмотреть скорость обратной реакции и вместо этого должны предположить, что wpz = w1. Мы называем эту реакцию необратимой.
Диффузия пептидов сгорания COO2 и H2O является незначительной, а также нет диспарталяции CHON/CO3, что только означает, что из этих веществ нет задержки. В результате необычно найти процессы сжигания, которые происходят в диапазоне температур ниже 1800-2000 гг.
Порядок реакции для определенного вещества представлен показателями степени (a и b) при концентрации реагирующих веществ в кинетическом уравнении.
Общий порядок, известный также как кинетический порядок, является общепризнанным общим порядком реакции.
Порядок реакции равен молекулярному порядку для простых химических реакций. Реакции на уровнях моно-, би- и тримолекулярных уровней вызваны передними или третьими позвонками.
Коэффициенты ab и b в своей сумме равны порядку реакции для отдельных компонентов, так как конечное стехиометрическое уравнение сложной реакции не отражает механизма ее протекания.
Экспериментально установленные коэффициенты, отражающие общий механизм протекания сложной многоступенчатой реакции, включают:
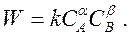
Коэффициенты, представляющие различные компоненты. Порядки отдельных компонентов в сложной реакции не соответствуют соответствующим стехиометрическим коэффициентам:
n = α β.
Концентрация реагирующих веществ является одним из факторов, который влияет на скорость реакции в процентах. Значение заказа может быть целочисленным или дробным, положительным или отрицательным, в зависимости от типа реакции и обстоятельств его курса.
Сложные реакции, которые протекают в несколько последовательных или параллельных стадий и производят как конечные продукты, так и другие побочные продукты, называются реакциями дробного и отрицательного порядка.
Скорость реакции в этом случае не зависит от концентрации вещества, что соответствует нулевому порядку для данного компонента. Для данного компонента реакция, в которой один из реактантов поддерживается в высокой концентрации, является примером реакции нулевого порядка.
Характеристики гетерогенного сжигания жидкости и твердого топлива влияют на то, как скорость зависит от концентрации реагентов.
Поток воздуха, полученный при сжигании жидкого топлива, непрерывно наполняется испарениями с поверхности жидкости. Поверхность частицы, покрытой топливом, остается постоянной и не влияет на то, как быстро сжигают жидкое топливо. Скорость сжигания варьируется в зависимости от концентрации окислителя.
На поверхностях частиц топлива, молекул и радикалов во время сжигания твердого топлива происходят химические реакции. Концентрация окислительного агента является единственным фактором, который влияет на то, сколько столкновений присваивается поверхностным единицам (как процент от общего числа). В этом случае единственным фактором, влияющим на скорость реакции сгорания, является изменение поверхностной концентрации окислительного агента.
Концентрация жидкости и твердого топлива постоянна во время гетерогенного сгорания. Кинетическое уравнение затем изменяется на следующую форму:
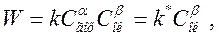
Где скорость гетерогенного горения?
Минеральные примеси и мелкие частицы других химических веществ, не участвующих в окислительно-восстановительных процессах, помимо активных горючих элементов, присутствуют в природном твердом топливе и ускоряют реакции.
Дата: 2022-07-30;Просмотр 698
§
Молекулярно-кинетическая теория утверждает, что химическая реакция – это процесс, в ходе которого разрушаются старые молекулы вещества и создаются новые молекулы.
Молекулы вещества движутся с разной скоростью в любом изолированном объеме при постоянной температуре. Только когда молекулы сталкиваются с большей энергией, чем требуется для разрыва старых внутримолекулярных связей, может произойти химическая реакция.
Многие, даже очень быстрые реакции не начинаются просто при контакте с реактивами. Смеси водорода и кислорода могут сохранять свою идентичность при комнатной температуре, в зависимости от температуры. Однако процесс начинается быстро (обычно со взрывом), как только к нему подносят горящую спичку.
Почему? Молекулы и другие химические частицы взаимодействуют при столкновении, но только продуктивным образом. Энергия активации EA конкретной реакции – это “пороговая” энергия, или минимальное количество энергии, необходимое молекуле для вытеснения сил внутримолекулярной связи. После получения этой энергии молекула готова превратиться в новое вещество.
Энергетический барьер, который необходимо пересечь, чтобы возникнуть реакция, – это то, что энергия активации может рассматриваться как.
Процесс реакции и энергия активации представлены на рис. 20.
Молекулы IDE в состоянии (1) имеют внутренний резерв энергии, E1, но недостаточно разбить молекулы перед ними.
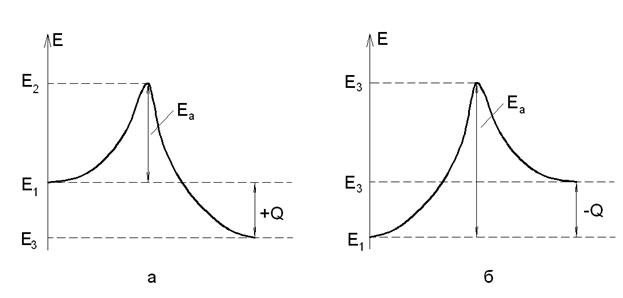
Рис. 20. Энергия активации реакции и тепловой эффект
Реакция, которая является экзотермической;реакция, которая является эндотермической.
Для возникновения прямой реакции необходимо подвести к системам определенное количество энергии EA. Это энергия активации прямой реакции. В данном случае молекулы переходят с внутренней энергией в состояние (2).
E2 = E1 EA.
Когда молекулы сталкиваются в состоянии 2, происходит химическая реакция с выделением и выделением тепла. Внутренняя энергия, выделившаяся при выделении E2, будет равна E3, а количество выделившейся энергии e1 – E2 после того, как продукты реакции остынут до начальной температуры (состояние 3).
Несоответствие энергии между той, которая высвобождается, и той, которая поглощается в процессе молекулярной активности.
Если эта вариация благоприятна (рис. 20а), t e 0, то происходит эндотермическая реакция; в противном случае – экзотермическая и эндотермическая реакции!
Прямая реакция, несомненно, является эндотермической.
Чем сложнее создавать реакцию, тем выше энергия активации. Как получить воздушный кислород для окисления углерода в воздухе?
C О2 = CО2
Согласно научным расчетам, что такое энергия активации?
ЕА = (25,6 ÷ 40) ккал/г-моль = (107000 ÷ 167000) кДж/кмоль.
На раскаленной поверхности углекислый газ может быть восстановлен при высоких температурах.
СО2 C = 2CО.
Какова энергия активации реакции?
EА = (32 ÷ 51,4) ккал/г-моль = (134000 ÷ 215000) кДж/кмоль.
Температура влияет на значение энергии активации. Количество энергии, необходимое для приведения молекул исходных материалов в активное состояние, уменьшается при повышении температуры, поскольку кинетическая энергия молекул уменьшается.
При низкой энергии активации в исходных материалах всегда будут присутствовать молекулы-компаньоны реакции. При высокой энергии активации внутри реактора может не оказаться ни одной молекулы. Энергия активации реакции уменьшается со скоростью реакции при прочих равных условиях.
Бывают ситуации, когда часто необходимо действовать с большой энергией. Конечно, вероятность такой реакции очень мала или почти равна нулю. Чтобы получить желаемый продукт, мы должны использовать “обходной путь”, если невозможно энергично нагреть реакционную смесь (например, потому что исходное вещество разлагается или равновесие смещается в пользу исходного вещества).
Дата: 2022-07-30;Просмотр 536
§
Скорость химической реакции зависит от температуры. Как правило, для начала активной реакции систему реагирующих веществ необходимо нагреть. В результате увеличивается количество так называемых “активных” молекул – тех, чья энергия активации выше энергии активации.
Статистический закон Максвелла-Больцманн гласит, что если молекулы имеют определенную энергию, то их число будет определяться этой энергией (рис. 21):
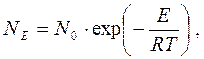
Общее количество молекул в единице объема – нет;
R – атомная газовая постоянная со значением 8,314 кДж/(кмоль-K).
Лишь небольшая часть молекул при низкой температуре T1 (заштрихованная область под кривой) имеет энергию, превышающую энергию активации EA. Поскольку они настолько малы, тепло, выделяемое каждой отдельной реакцией, не может значительно повысить температуру смеси.
Энергии молекул (заштрихованная область под кривой t2) умножаются в результате повышения температуры до T2, что позволяет нам предсказать активную реакцию с коэволюционной скоростью.
Естественно, химическая реакция может продолжаться при более низкой температуре с более низкой энергией активации. Скорость химической реакции увеличивается вместе с количеством «активных» молекул.
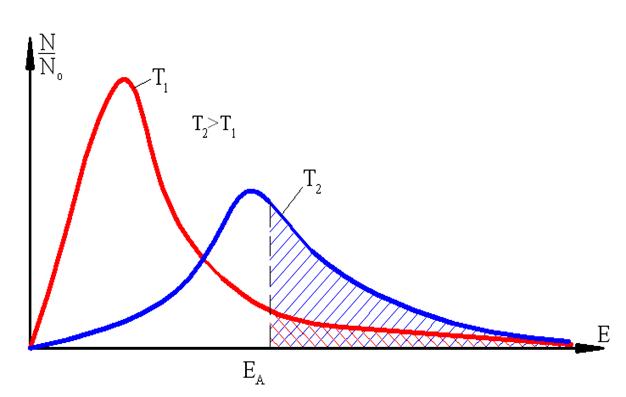
Рис.21. Максвелл-Болцман Статистики
Число частиц с силой E EA равно сумме этих двух величин, согласно закону Максвелла-Больцмана, который описывает распределение молекул в зависимости от их кинетической энергии (EA).
В качестве частного случая общего закона Максвелла-Больцмана применительно к химическим реакциям шведский ученый Сванта Аррениус в 1889 году установил зависимость скорости реакции от температуры (Рис. 22).
Закон, установленный Аррениусом, устанавливает связь между скоростью химической реакции k и температурой t:
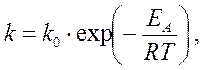
Коэффициент пропорциональности, известный как k0, описывает, как часто сталкиваются все реагирующие молекулы в данном объеме.
Рис.22. Аррениус ‘
Кинетическая теория, которая по сути является квадратным корнем из значения температуры, утверждает, что число столкновений зависит от скорости свободного пробега молекул. Согласно этим цифрам, частота столкновений изменяется на 10% между 200 и 300 C.
Множитель отображает процент всех молекулярных столкновений между “активными” молекулами, которые приводят к реакции.
Более того, если концентрации исходных веществ остаются постоянными, скорость реакции будет увеличиваться, поскольку константа скорости реакции растет с повышением температуры.
Одним из фундаментальных уравнений химической кинетики является закон Аррениуса, а энергия активации является важным количественным показателем реактивности вещества.
Возьмем для примера сжигание углеродного топлива с выделением углекислого газа, которое происходит при энергии активации E=125000 кДж/кмоль и температуре 1000 K.
Соотношение скоростей реакции будет, если мы начнем с ko=const.
Wp1500 / Wp1000 = exp(–125000/(8,314∙1500))/exp(–125000/(8,314∙1000)) =
= еxp(–10)/еxp(–15) = еxp(5) = 145.
Увеличение скорости становится слабее при повышении температуры реакции. В результате, при повышении температуры на 500 C соотношение скоростей выглядит следующим образом:
Wp2000 / Wp1500 = exp(–7,5) / exp(–10) = exp(2,5) = 12,2.
Величина предэкспоненциального множителя K и скорость молекул одновременно увеличиваются в результате повышения температуры.
ko1500 / ko1000 = (1500 / 1000)0,5 = 1,22.
Температура оказывает влияние на количество реактивных молекул и их столкновений, а КО не пропорциональна температуре.
Общее увеличение скорости детали будет высвобождаться с учетом изменения КО в реакции:
Wp1500 / Wp1000 = 145∙1,22 = 177.
Пример показывает, как влияние роста температуры на скорость химической реакции постепенно уменьшается, и скорость реакции стремится к установленному минимуму.
Это следует, по крайней мере, из того же анализа зависимости от значения ret, даже если мы начнем с анализа зависимости exp(-E\/(RT)).
если Т→ ∞, то величина exp (–Е/(RT)) → 1, а k → ko.
Следовательно, на кривой exp(-E/RT)=f (T) должен существовать перегиб.
Скорость химической реакции увеличивается до изгиба, как и функция, однако после избыточного роста она ослабевает и асимптотически приближается к постоянному значению.
Вычисление точки перегиба предполагает приравнивание второй производной к нулю. RT/E = x, далее следует функция y=exp(1/4x);
y” = d2y / dx2 = ((1–2x)/x4) exp(–1/x) = 0 .
Это приводит к выводам, что x = 1/2 и TPEP – E (2).
Если сжигание углерода происходит в термодинамическом режиме при E = 125000 кДж/кмоль, реакция сжигания углерода происходит следующим образом.
Тпеp = 125000/(2∙8,314) = 7517 К.
Точка экстракта значительно выше, чем фактические температуры для всех важных для нас реакций.
Мы обращаемся к области кривой, где резко увеличивается скорость реакции.
Дата: 2022-07-25;Просмотр 1401
§
Сложный физико-химический процесс горения основан на химической реакции окислителя и горящих веществ.
В реальных условиях скорость потока горючих веществ, а также скорость образования горючей смеси (скорость распада смеси) определяет интенсивность горения.
Учение о механизмах парообразования и законы химической кинетики определяют, как быстро протекает химическая реакция. Скорость образования смеси больше, чем скорость молекулярной диффузии. В этом случае скорость самой медленной фазы будет определять конечную скорость процесса горения.
Если скорость обращения с горючей средой в течение указанного периода времени значительно медленнее, чем скорость химической реакции между горючим и окислителем. Такой Гром имеет движение.
Процедуры диффузии не превышают 15%, если скорость подачи окислителя в сгорание значительно ниже, чем скорость химической реакции. Диффузионное сжигание – это термин, используемый для описания этого процесса.
На рисунке 23 показана зависимость между скоростью горения и температурой процессов интенсификации при различных условиях разговора.
Взаимодействие КСИМИХИЧЕСКИХ ФУТОВ-ДЮЙМОВ с молекулами WX и GOSHY. R окислитель при повышении температуры.
Транскрипция туропилапной диффузии присваивает себе расход ВСМ; она не определяет температуру.
Скорость химических реакций намного медленнее в области низкой температуры (T1 на графике), чем в других областях. При сравнительно низких температурах можно увидеть кинетическое сгорание. Только в условиях чрезвычайно энергичной циркуляции может происходить кинетическое сгорание.
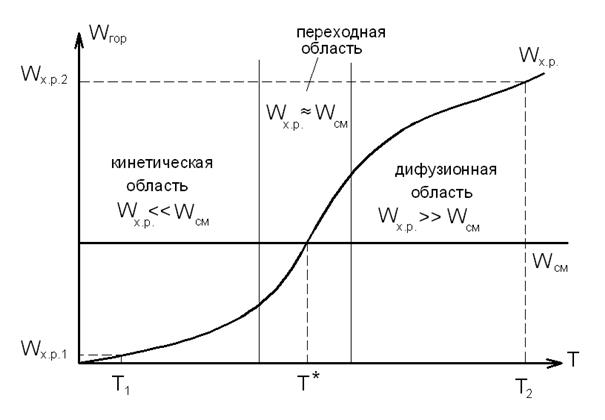
Рис. 23. Кинетическая и диффузионная области горения
Если мы сравним скорость смесей в области высокой температуры (на графике, T2) с скоростью химической родовой реакции, скорость смесей умножается много раз. Сжигание происходит в области диффузии на более глубоком уровне. В зоне сгорания диффузное сжигание обычно наблюдается при подходящих температурах. При низких температурах это верно в медленном смысле.
Следующие конвенции применимы к кинетической и диффузионной гопении: подростковый возраст XmicishiCair – значения того же порядка (Tempa T*). Это Гования, которую питается диффузией и кинетическими про-камами.
Как иллюстрация сжигания твердого топлива. Как правило, на ранних стадиях реакции, когда температура реакции все еще низкая, скорость реакции низкая, или избыточный кистидж присутствует в области вокруг реакции. Процесс сжигания в этом случае сопровождается медленной скоростью химической редакции, то есть кинетикой реакции. Процесс сгорания не повлияет на улучшение аэродинамики печи или увеличение снабжения кистера до горящей частицы. Это кинетическая территория сгорания.
Химическая реакция усиливается при высоких температурах и потребляет значительное количество кислорода. Скорость сжигания затем уже определяется скоростью диффузии окиси углерода из зоны разложения, когда концентрация кислорода на поверхности частицы начинает быстро падать.
Возможность оценки гопения по кинетическим и диффузионным показателям отрицательно сказалась на исследованиях механизмов горения, поскольку позволяет не принимать во внимание другие факторы.
7.5. Еще одна интерпретация «кинетического сгорания путем диффузии».
Чаще всего для осуществления процесса сжигания топлива используются приборы (такие как печи, духовки и т.д.). с невероятно сложными аэродинамическими свойствами. Кроме того, ни одно современное топочное устройство не может гарантировать идеальное (на молекулярном уровне) смешивание топлива и окислителя. При достаточной активности компонентов горючей смеси химическая реакция протекает в соответствии с законом Аррениуса с такой значительной скоростью при высоких температурах и концентрациях исходных компонентов (горючего или окислителя).
Три фактора, в целом, составляют общее время горения горна:
Количество времени, необходимое для физического контакта топлива и окислителя (при сжигании газа – время смешивания), см. рис.
Сроки достижения температуры воспламенения горючей смеси
Хим: время реакции в атомах
τгор = τсм τнаг τхим.
При каких обстоятельствах одна и та же процедура (смешивание и нагревание) может определять общую скорость сгорания?
В силу законов молекулярно-ирритивной диффузии процесс смешения подчиняется законам молекулярно-кислотного перехода, если не учитывать время, необходимое для разогрева и протекания химической реакции.
Сгорание неподготовленной газовой смеси является одним из примеров такого процесса. В случае, если подача воздуха не смешивается с окислителем. В печи смешивание уже происходит в объеме зарядки, а время, необходимое для образовательной смеси, намного длиннее, чем время, которое необходимо для химической реакции.
По мере развития процесса горения в диффузионной области выделяется большое количество удельного тепла.
Если время нагрева и смешивания одинаково! Следовательно, практически это означает, что у нас остается только кровь. Скорость химической реакции, как мы все знаем, играет важную роль в скорости горения. В результате процесс протекает в кинетической области.
Когда при температуре под температурой зажигания добавляется однородная, устойчивая к зажиганию смесь при температуре ниже температуры зажигания. Когда сжигание происходит в кинетической области в течение начального периода, когда температура все еще низкая.
Например, кинетические и диффузионные принципы могут быть использованы для объяснения того, как топливо сжигает в воздушном потоке.
Кинетический принцип отличается от кинетического тем, что предполагает предварительное приготовление однородной смеси топлива и воздуха. В однородной среде горение протекает с постоянной теплоотдачей и избытком воздуха (r=const).
Материалы, опубликованные в Интернете, которые нарушают авторские права
§
Процесс сгорания газа происходит на основе теплофизических характеристик отдельных компонентов. При нагревании при высоких температурах без воздуха термостабильные вещества, такие как CO и H2, сохраняют свою молекулярную структуру. Большинство насыщенных углеводородов из ряда метана, например, при нагревании в отсутствие воздуха разлагаются с образованием более легких соединений и атома углерода. По мере увеличения молекулярного веса углеводородов температура, при которой начинается термическая диссоциация этих веществ, снижается. Метан CH4 обычно начинает термически разлагаться при температуре 600-800 оС, а этан C2H6 – при 400 оС.
Если окислителя недостаточно для полного окружения газа (1) или если смешивание происходит неорганизованно.
Сложная цепь превращений, приводящая к пиролизу природных газов, содержащих определенное количество тяжелых фракций. Для представления термического разложения метана можно использовать следующую схему:
СН4 СН2Н2
С Н2СН4,С Н6
С2Н6 С2Н4Н2
С2Н4 С2Н2Н2
С2Н2 2С Н2
——————————
2СН42С4Н2
Четыре свободные связи между атомами углерода, высвобождающиеся при пиролизе, позволяют им соединяться друг с другом и образовывать твердые кристаллы графита при отсутствии кислорода. Они горячие и образуют блестящий факел в области активного горения. Температура, при которой воспламеняется газ, немного ниже температуры, при которой происходит термическое разложение углеводородов. Все молекулы топлива, вступающие в контакт с количеством атомов окислителя, необходимым для полного сгорания, образуют относительно небольшое количество частиц углерода при хорошем смешении. В результате длина светящейся части факела не имеет значения.
Ухудшение процесса смешивания замедляет и задерживает сгорание твердых частиц сажи. Факел выглядит растянутым и длинным. Это приводит к потере тепла, так как сажа попадает в зоны с низким уровнем кислорода и не сгорает. На поверхностях нагрева также образуется жировая сажа, которая служит дополнительным источником тепла.
Какая возможная чистота существует в саже, образующейся при термическом распаде топливных углеводородов? В зависимости от того, сколько газов в ее составе содержат углерод и водород (2).
.
Для утверждения цен на газ C/N 3.0 необходимо
Результаты воздействия метана и водорода не совпадают с тем, как на самом деле разворачивается процесс. Механизм горения газа на самом деле более запутанный и хаотичный. Присутствует множество промежуточных химических реакций (превращений), которые обычно являются цепными реакциями.
В качестве обоснования вы можете привести нарушение авторских прав.
§
Тот факт, что газовое топливо смешивается с окислителем, оказывает сильное давление на полноту сгорания (ПАМП, КОМПЬЮТЕРЫ), а также на КСАПКТАТИЛИСТИКУ ФОРЕЦ ПЕПЕКАЛЬНОЙ ЭКСТРАКЦИИ. Окислительные пестроты страдают в результате неправильного заражения топлива воздухом. Факторами риска являются неполное сгорание (ксимический недожог) и протежирование углеводного деления Теппи. Коэффициент избытка воздуха в топке должен быть повышен в случае химического недожога, при пухлости, что также относится к поту с отходящими газами.
Горелки используются для сжигания топлива. Они сделаны так, чтобы обеспечить камеру сгорания необходимым количеством топлива и окислителя для заданной производительности устройства (или наоборот). Для этого используются различные позитивные методы.
Устройство для подачи газа и воздуха, камера смешения (топлива или окислителя) и механизм конвектора являются общими конструктивными элементами всех газовых горелок. Конструктивное исполнение элементов горелки может варьироваться в зависимости от назначения, области применения и технологических требований. Например, некоторые компоненты могут отсутствовать или могут быть объединены.
При сжигании топлива в качестве высокого калорий, как природный газ (СПГ), конструкция и аэродинамические свойства устройств горелки имеют первостепенное значение.
Горелка также функционирует как компонент системы для формирования смесей и создания стабильного фронта зажигания в устье горелки, чтобы воспламенить смеси газовой воздушной воздушной эфир, которая возникает из нее.
Независимо от того, совмещены или разделены процессы образования смеси и нагрева до температуры воспламенения, горение газа обладает принципиально разными свойствами.
Существует три фундаментальных принципа организации для процесса сгорания, в зависимости от того, как газ и окислитель (воздух) подаются в камеру сгорания:
Принцип внешнего смешивания гласит, что когда газ и воздух подаются в gorenje раздельно (в виде отдельных струй или потоков), смешивание происходит непосредственно за срезом горелки.
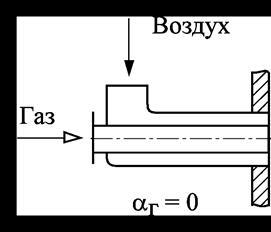
Рис.24
2) принцип полного внутреннего смешения, когда газ со всем эжектируемым или принудительно подаваемым воздухом, необходимым для горения, смешивается непосредственно в пределах горелки, при этом в зону горения поступает однороднаягазовоздушная смесь (кинетическое горение) – горелка с полным предварительным смешением – αг > 1
(рис.25);
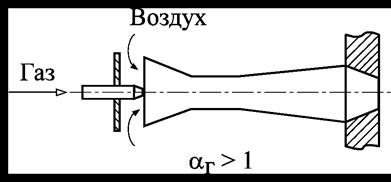
Рис. 25. Полное предварительное смешение на горелке.
3) принцип частичного внутреннего смешения, когда газ смешивается в пределах горелки лишь с частью воздуха, необходимого для горения (первичный воздух), а остальная часть воздуха (вторичный воздух) подаётся в топку отдельным потоком. Окончательное смешение происходит уже в топочном объёме совместно с процессом горения –
горелка с частичным предварительным смешением– αг < 1 (рис.26).
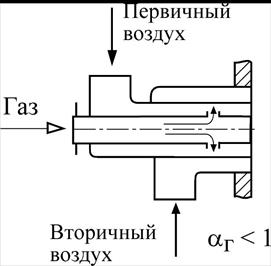
Рис. Горелка с частичным предварительным смешением, место 26
Наряду с этими тремя основными принципами, возможен и очень часто практически реализуется промежуточный, или смешанный, принцип сжигания газа – принцип неполного предварительного смешения,
когда предварительное смешение газа с воздухом находится на стадии неполного завершения (причём степень этой незавершённости может быть самой различной), т.е. в зону горения подаётся неоднороднаягазовоздушная смесь.
Процесс сгорания газа может сопровождаться образованием короткого факела или длинного факела, в зависимости от техники, используемой для создания смеси для сжигания, и конкретной конструкции горелки.
Они сжигают в растянутой вспышке до тех пор, пока они полностью или частично смешаны. При сжигании газа с высоким содержанием углеводородов и локальной нехваткой воздуха вспышка часто светительна. Нефтяные горелки – это те устройства, которые испускают ясную вспышку.
Процесс смешивания заканчивается за пределами объема факела при горении предварительно перемешанной газовоздушной смеси. Кроме того, в гомогенном факеле огонь тусклый и горение протекает быстро, прежде чем полностью закончиться на небольшом участке. Это приводит к значительному увеличению полноты сгорания и снижению необходимого коэффициента избытка воздуха. Так называемые горелки для предварительной смеси лишь иногда называют пламенем.
В то время как смешивание и горение происходят одновременно в реакционном объеме диффузионных горелок, процесс образования смеси является ограничивающим. Причиной этого является большая длина диффузионной горелки по сравнению с гомогенной.
Размер диффузионного факела изменяется в зависимости от температуры смешивания. Можно добиться уменьшения длины зоны смешения или увеличения ее размера, т.е. изменить свойства диффузионного факела
Что замедляет процесс горения газообразного топлива – скорость химической реакции, т.е. кинетика или скорость смешанного образования (диффузия)? Где происходит горение газа? Какой из двух основных факторов, характеризующих скорость процесса горения, является определяющим?
Скорость высвобождения тепла в зоне сгорания и время сгорания представляют собой формулы, которые можно использовать для помощи в этих запросах.
В соответствии с моделью Я. Согласно модели Б. Зельдовича, тепловое напряжение в зоне реакции горения определяется по следующей формуле:
,
И продолжительность горения выделенного элемента в зоне реакции
,
Типичная скорость пламени, распределенная в стационарной среде, u n = 0,35 м/с, определяется плотностью и теплопроводностью смеси газовой воздушной системы на выходе горелки. Начальная температура газовой системы с воздухом внутри нее (в зоне реакции), а также коэффициент температуры газа, когда она снижается до углекислого газа или воды, является T0 в теории сжигания. Поскольку топливо нагревается источником тепла через стены котла, чтобы охладить их под давлением около 450 атмосфер, давление воздуха упадет в случаях увеличения давления.
Он горит быстро и при высоких температурах с эффективным молекулярным смешиванием газа и воздуха:
Интенсивность тепловыделения, с
Какое время горения?
Есть места, где газ и воздух смешиваются при воспламенении огня. Скорость химической реакции, которая регулируется законами кинетики (химии), является тормозящим фактором; горение происходит в чисто физической среде. Однако из-за высокой интенсивности горения и потребления кислорода готовая смесь быстро расходуется, что требует более интенсивной подачи воздуха в зону горения для поддержания процесса горения.
Кроме того, важно помнить, что в процессе горения в смесь вводится третий компонент. При добавлении инертных компонентов конечная смесь “разбавляется”, что затрудняет столкновение молекул топлива и окислителя.
Например, скорость образования смеси в диффузионной области может замедлить скорость горения газа при высоких температурах.
Согласно исследованию, скорость кинетического горения в правильно функционирующих горелках достигает скорости смеси при температуре 1000 ОС. Улучшение аэродинамики горелок необходимо для ускорения горения.
Конструкция газовых горелок должна, прежде всего, естественным образом связывать устройство всей топочной камеры и гарантировать следующие функции:
Количество газа и воздуха, необходимое для того, чтобы зона горения пережила лето.
Смешивание газа с воздухом по выбранному принципу;
Почти полное сгорание газа (за исключением редких случаев, когда в процессе работы топочной камеры требуется восстановительная среда);
Установление необходимой температуры в печи и камере gorenje;
Обеспечьте необходимую излучательную способность пламени.
Разнообразный диапазон газовых горелок требует их классификации в различных, отчетливо разных группах.
Различные черты могут быть использованы для чего -либо классификации. Ни один из классификационных атрибутов не является одиноким и не может адекватно описать каждый основной аспект проекта и эксплуатации газовой горелки. Техническая литература настоящего не имеет единой классификации.
Ряд дизайнерских элементов присутствует в горелках, созданных для комбинированного сжигания газа и других видов топлива (таких как мазут или угольная пыль).
Горелки также могут быть классифицированы с использованием определяющих принципов или атрибутов классификации.
сжигаемое топливо;
) как подают воздух;
Какой тип стока происходит;
формы устья горелки (геометрия);
) способ завихрения (крутки);
способ регулирования крутки потоков
давление газа;
скорость истечения;
степень автоматизации;
· прочие.
Горелки делятся на две группы на основе метода подачи воздуха:
Вдуватели (дутьевые горелки);
В виде выброса воздуха с газовым чипом.
Прямоточные и вихревые горелки – это два разных типа продувочных горелок, в зависимости от характера выходящих потоков.
Структура факела в прямоточных горелках определяется формой устья, которое может быть прямоугольным.
Тангенциальные (Т) и аксиальные (А) лопастные завихрители являются наиболее часто используемыми лопастными завихрителями в вихревых горелках.
Для регулирования салфеток потоков можно использовать следующие методы:
изменение угла наклона лопаток;
Путем изменения живого сечения лопаточных вихрей или сечения входного сопла;
Путем исключения части потока воздуха, проходящего через завихритель.
Изменение максимальной скорости вдоль оси струи, изменение максимальной скорости обратного тока и профили скорости (осевые, тангенциальные или радиальные) являются основными аэродинамическими характеристиками закрученных струй.
На форму пламени и интенсивность тепло- и массопереноса влияют параметр закрутки, геометрия горелки и отношение скоростей первичного воздуха.
Параметр поворота можно рассчитать с помощью параметров конструкции поворотной машины.
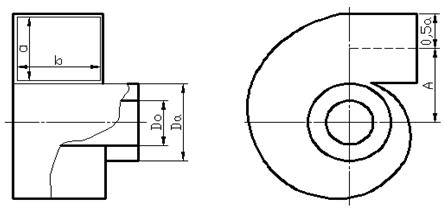
Б) улиточный
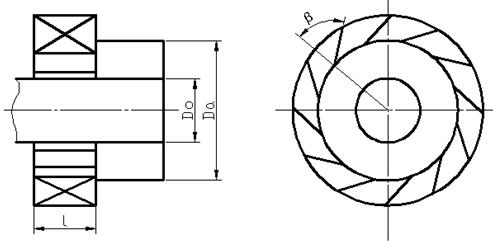
А) тангенциальный лопаточный
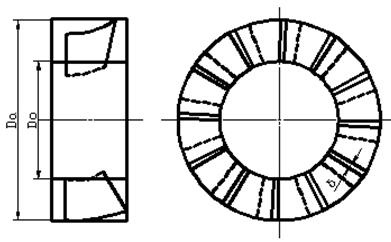
В) аксиальный лопаточный
Рис.27. Как действуют завихрители?
Следующие характеристики вихревых струй представляют особый интерес для технологии печей:
На основе этого распределения формируются вектор скорости и статическое давление;
Максимальные скорости по длине струи;
Объем рециркуляционных газов и размер зоны обратного течения;
диаметр струи;
увеличение массы струи.
Интенсивность процесса смешивания может варьироваться в зависимости от того, как объединяются топливо и окислитель.
увеличение скорости потоков;
Подача потоков, пересекающихся под углом
Смешивание потоков по отдельности и их дробление.
К стабилизаторам относятся стены, плохо обтекаемые тела и конические поперечные сечения;
Применение предполагаемого «резкого взрыва», то есть.создание турбулентности в основном потоке, вызванном введением быстрых дополнительных воздушных самолетов;
закручивание потоков воздуха.
Дата: 2022-07-30;Просмотр 1039
§
Сгорели и кислород объединяются в процессе горючих и окислителей. Тип сжигания, длина и излучательность вспышки и уровень сжигания газа зависит от смешивания.
Как уже было сказано, в зависимости от конструкции горелки процесс сжигания газа может сопровождаться образованием короткого или длинного пламени. При соединении компонентов в камере сгорания сгорание происходит в вытянутом факеле, который светится. Факел, возникающий при сжигании предварительно смешанной газовоздушной смеси, короткий и не светится.
Поскольку процесс смешивания газа и окислителей происходит при взаимодействии потоков, процесс образования смеси имеет значительную сложность.
Когда топливо и окислитель вводятся в камеру сгорания по отдельности, влияние смешивания на процесс горения особенно очевидно. Горючая смесь может быть создана таким образом, например, путем нагрева газа и/или воздуха до температуры чуть ниже температуры воспламенения. Предварительное смешивание не подходит, поскольку это привело бы к воспламенению смеси еще до того, как она попала в камеру сгорания. Это создает дополнительные условия, но в том же случае позволяет увеличить длительность факела.
Основная задача рациональной газовой горелки заключается в изменении излучательной способности факела и качества смешения.
Интенсификация процессов смешивания в газовых горелках происходит двумя путями
2) Путем разделения больших потоков на более мелкие;
3) увеличение размера и интенсивности турбулентности (изменение закрученных потоков).
Во-первых, следует повлиять на процесс горения, добавив аэродинамику в область, где впервые образуется факел. В статье рассматривается аэродинамика потока топочного газа, турбулентные процессы теплообмена и масса в камере сгорания.
Каждая горелка должна гарантировать надежное зажигание и стабилизацию фронта пламени. Стабилизация пламени – это процесс создания условий, гарантирующих непрерывное зажигание пламени без ударов и пульсаций.
Если факел находится близко к рту горелки и остается в своем типичном положении в космосе, говорят, что он стабилен. Взаимодействие между скоростью распределения пламени и противодействием значения смеси газо-воздуха, возникающей из уст горелки, приводит к этому состоянию факела. Феномен огня, втягивающегося на горелку, невозможно, если скорость потока смеси газо-воздуха превышает скорость распределения пламени. Из-за рециркуляции продуктов сгорания в основу факела, скорость истечения смеси газовой смеси также слишком высока, что не дает ей времени нагреться.
На рис. 28 показаны качественные границы устойчивости пламени в зависимости от степени аэрации горючей смеси, коэффициента избытка воздуха в первичной фракции и скорости коагуляции газа с воздухом.
Нижний предел стабильности горения колеблется по кривой, напоминающей закон, согласно которому концентрация газовоздушной смеси влияет на скорость горения. По мере увеличения количества гор максимальное устойчивое горение резко уменьшается.
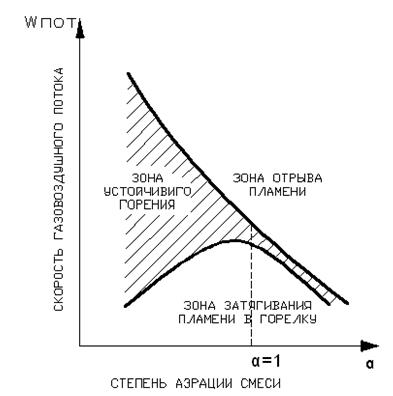
Рис. 28. Границы для стабильности пламени в зависимости от фаз
Что отличает скорость от избытка воздуха?
Как называется выход газоотвода из горелки?
Только при небольшом количестве первичного воздуха в исходной смеси горение происходит в широком диапазоне скоростей. В этом случае стабильность горения обеспечивается надежным источником запального пламени – диффузионным шлейфом, который образуется в камере во время газового пожара. Гор увеличивается при увеличении доли первичного воздуха, так как влияние диффузионного фронта пламени нивелируется. При гор = 1, то есть когда диффузионное горение отсутствует вообще или наблюдается только в очень малом диапазоне изменения скорости газовоздушного потока (рис. 1)
В этих обстоятельствах необходимо повысить температуру зоны воспламенения газовоздушной смеси, например Чтобы пламя не вырывалось из горелки, завихрите потоки.
8.5. Как рассчитываются газовые горелки?
В связи с неоправданной сложностью точного расчета газовых горелок, на практике были разработаны многочисленные методы аппроксимации.
Газовые горелки, которые пересекают воздушный поток в поперечном направлении мелкими газовыми струями, являются наиболее распространенными на электростанциях.
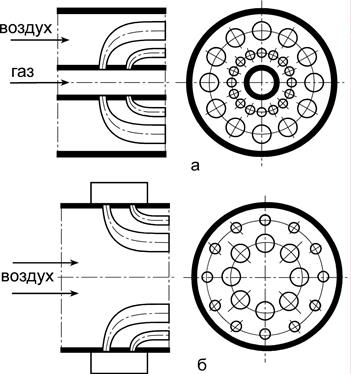
Рис. 29. Схема подачи газа в поперечном воздушном потоке
В середине;б, поступающий с краев.
Эти потоки подметают газовые струи, когда они пронзит воздушный поток. Осевая линия газовой струи будет совпадать с направлением воздушного потока после того, как достигнуто заранее определенное расстояние от стенки газового коллектора H. Соотношение скоростей газа и воздуха (WR, WV) и диаметра сопла струи дрейфующей струи (DC) определяют глубину проникновения струи в дрейфующий поток. Сотены построены в два ряда для улучшения распределения газовых струй по поперечному сечению горелки и более однородному смешиванию газа в воздухе.
Основываясь на многочисленных экспериментах Ю, фундаментальной формулой для расчета таких горелок является зависимость от относительной глубины проникновения струи газа в поперечный поток воздуха:
, (13)
Что касается относительного шага между соплазами подряд, KS является эмпирическим коэффициентом.
Примерное описание геометрии газовых струй, выходящих в поперечный поток воздуха, показано на рис.30.
Траектория струи искривляется под действием воздушного потока, а диффузионное размывание приводит к увеличению струи. Размещение отверстий для выхода газа должно обеспечивать перекрытие струй в поперечном сечении (там, где они принимают направление потока) по всему сечению.
Вы должны заранее задать значения скоростей газа и воздуха и на основании советов из опыта при расчете газовых горелок определить глубину проникновения струи.
Рис. 30. Схема распространения струй газа
В поперечном потоке воздуха
Внутренний диаметр din трубы газоснабжения определяется уравнением потока газа:
.
Чтобы определить скорость газа, нажмите кнопку в трубу. Совещаются значения WP. TR от 20 до 30 м/с.
По уравниванию расхода воздуха
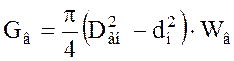
Определите внутренний диаметр наружной трубы подачи воздуха Din, а затем выберите подходящую трубу из имеющихся вариантов (dp – внешний диаметр газопровода).
При определении расстояния, на которое могут проникнуть струи газа, выходящие из сопел разного размера. В области, где условный диаметр газовых струй и оси, повторяющие направление воздушного потока:
Dстр=0,75Hиdстр=0,75h .
Согласно плану распределения струй в кольцевом канале (см. Рис. 13) из этого следует, что глубина проникновения мощных самолетов:
→ → ,
а малых:
→ → .
Диаметры большой и малой дроби рассчитываются по формуле (13), где KS = 16:
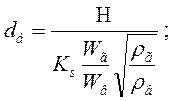
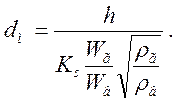
. Определите геометрический состав горелки, если в соответствии с рекомендациями центральное газоснабжение подается на 20% через малые или большие сепары и на 80% через большие сопла:
Объединенный размер двух размеров сопли
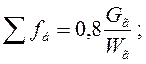
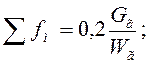
Какова доля сопливых, которые бывают большими и маленькими?
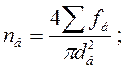
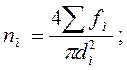
Процесс установки больших и маленьких сопел.
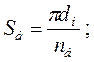
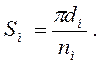
Формула Хоттеля определяет размерность факелов
,
Где ТА обозначает адиабатическую температуру и начальную температуру газа?
Дата: 2022-07-25;Просмотр: 1033
§
Несмотря на общую тенденцию использования меньшего количества жидкого топлива (в первую очередь мазут), он по -прежнему имеет множество применений. В этом случае скорость испарения растет вместе с соотношением частиц к частицам от частиц и капли, а также количеством теплового входа.
Под действием тепла газов капли жидкого топлива (например, мазута) быстро нагреваются, попадая в камеру сгорания или топочную камеру котла. Сначала испаряются легкие фракции. В результате температура горения и температура воспламенения оказываются выше точек кипения различных фракций жидкого топлива. Под действием тепла топливо испаряется с поверхности, в результате чего его пары нагреваются и сгорают. В результате жидкое топливо сгорает в парогазовой фазе. Видимая искра находится далеко и никогда не касается поверхности.
Излучение играет меньшую роль в процессе нагрева капли, чем конвективный компонент теплопередачи.
Критериальное уравнение описывает теплопередачу при течении вокруг небольшой сферической капли в области низкого числа Рейнольдса (Re 2):
Nu = 2 0,6∙Re0,5∙Pr0,33 ≈ 2
или , т.е.
В результате количество тепла, передаваемого конвекцией, увеличивается по мере уменьшения размера капли.
Коэффициент теплопередачи газа составляет 0,144 Вт/(мс) при температуре дымовых газов 1400 С.
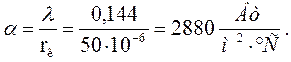
Инжир. Схема горения капли жидкого топлива (рис. 14)
Топливо испаряется во время нагрева, образуя облако пара, которое рассеивается в окружающем воздухе. Поскольку пары горючего топлива и кислород находятся в стехиометрическом соотношении вдали от капли, смесь воспламеняется от тепла дымовых газов, которое выше температуры пламени высококипящих фракций. Фронт горения паров топлива находится здесь и образует сферу вокруг капли.
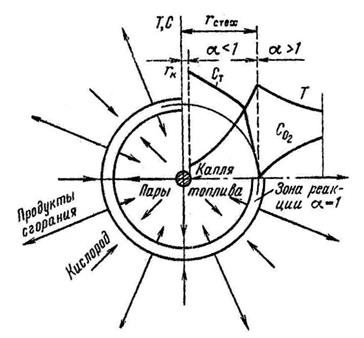
Рис. Диаграмма сгорания капли топлива, страница 31
В результате испаряющаяся капля (ddor) оказывается окруженной полой сферической поверхностью горения.
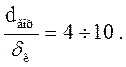
Из-за тепла, затраченного на нагрев и испарение топлива, температура горения повышается в зоне реакции, а затем снижается в пределах сферы.
Скорость химической реакции и скорость диффузии кислорода в зону горения – два из трех основных факторов, влияющих на интенсивность горения капли жидкого топлива. Из-за чрезвычайно высокой скорости химической реакции в газовой фазе горение невозможно замедлить. энергии кислорода, диффундирующего к фронту горения пламени через поверхность шара. Таким образом, поверхность фронта горения и массовое поступление кислорода увеличиваются даже незначительно за счет смещения зоны горения от поверхности капли. Испарение жидких фракций топлива происходит медленно в начале горения, до воспламенения, когда температура еще не достигла критической точки. В этом случае на интенсивность испарения помимо температуры влияет размер поверхности. После воспламенения температура поверхности капель быстро повышается, испарение усиливается, а скорость горения замедляется из-за недостатка кислорода.
В реальных условиях скорость сгорания жидкого топлива определяют два процесса – интенсивность испарения и диффузия кислорода в зону сгорания.
Топливный пара вытесняет воздух из межпоточного пространства в начале Gorenje в более высоких концентрациях смеси топливного воздуха. В результате развиваются области с низким уровнем кислорода, а нагревание приводит к высвобождению асбеста. Факел, по -видимому, ярко светится в результате более длительного, гетерогенного процесса Gorenje частиц сажи.
В следующих формулах используется уравнение для определения теплового баланса испарения капли:
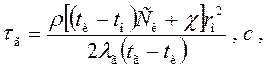
Средняя теплоемкость жидкого топлива измеряется в кДж/(кг С); начальный радиус капли жидкости измеряется в м; а температура поверхности капли измеряется в оС. Плотность воды у нефти выше, чем у газа, использующего тепло от раскаленного до холодного водорода при комнатной температуре (420 Кельвинов). Для сравнения Tg – теплопроводность газов в атмосфере – достигает 360 градаций по шкале Мооса на 1 градус ниже нуля C.
Время полного испарения, вероятно, в значительной степени зависит от размера капель. Крупные капли аэрозоля также дольше испаряются и представляют угрозу для шлейфа.
На рисунке 32 изображена структура факела при сжигании жидкого топлива.
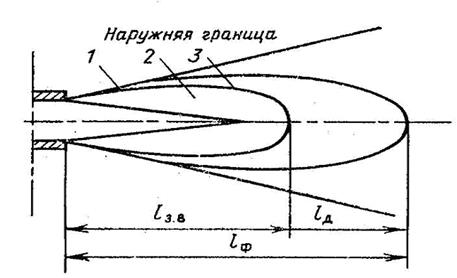
Рис. 32. Иллюстрация факела жидкого топлива
1 – зона воспламенения; 2 – область испарения и образования горючей смеси;
Lз.в – длина зоны воспламенения;
Id – длина зоны дожигания, f – скорость пламени.
Зона зажигания 1, которая находится за пределами зоны огня, – это то, где горит большинство парообразных углеводородов. Зона зажигания обычно разделена на две области: внутренние 2, где проводятся процессы испарения воздуха, а также горючие формы смеси, а также внешние 3, где изгнаны продукты горячего сгорания.
Наиболее ответственным этапом в приготовлении жидкого топлива является его распыление до мельчайших частиц технологического оборудования, так как интенсивность горения увеличивается с ростом, что влияет на его количество в частицах (фоферсунах). Например, при дроблении капли диаметром 1 мм может образоваться 106 капель. При таком сценарии площадь поверхности испарения увеличивается в 600 раз.
Размер капель, образующихся при распылении жидкого топлива, варьируется от 5 до 500 микрон. Самые маленькие капли первыми испаряются, вспыхивают и загораются. Важно помнить, что механизм горения жидкого топлива включает промежуточные комбинации и зависит от образования окислителя в горючей смеси. Оно легко разлагается на водород H2 и монооксид углерода CO при достаточном количестве окислителя (который, в свою очередь. параграф 8.2).
В реальных условиях отдельные лучи факела имеют разную температуру. Углеводороды подвергаются термическому разложению при недостатке окислителя. Характер этой процедуры зависит от температуры. При относительно высоких температурах возможно образование тяжелых, несвязанных углеводородных комплексов в сажевые углеводороды.
CmHn → mC 0,5nH2 .
В этом случае смесь легких парообразных и газообразных углеводородов, тяжелых жидких углеводородов или даже твердых теплоносителей может составлять горючую часть факела мазута.
Воздух, необходимый для горения (например – факельный дым), используется для остановки процесса сгорания тяжелых углеводов и сажи. Очень важно тщательно соединить воздух с горючими частями факела.
Для этой цели используются вихревые горелки. На рис. 1 сравниваются профили осевой составляющей скорости и реальная форма факела. У незакрученной струи (см. рис. 13 13, кривая a) струя расположена на выходе из устья горелки и находится далеко от звезды; она имеет конусообразную зону зажигания. У изогнутой струи (см. рис. 1, кривая б) за счет падения давления в середине факела и разрежения при сверхкритической закрутке, которое отсчитывает высокотемпературные продукты горения плазмы на поверхности земли или в газовом пламени и увеличивает скорость распространения тепла по земле, возможно снижение давления до 10-кратного минимума к полудню после того, как температура воздуха достигнет максимального для человека значения. В этом случае происходит более интенсивный процесс горения, помимо внутреннего внутреннего горения струи и воспламенения ее внешней поверхности.
Дата: 2022-07-30;Просмотр 1635
§
В зависимости от способа распыления жидкого топлива форсунки можно разделить на три сложные категории: механические (рис. 33, 34), с диспергирующей средой (рис. 36) и комбинированные 37).
Механические форсунки подразделяются на трудитиры под различными названиями:
Прямоточная форсунка: Распыление происходит потому, что топливо имеет энергию перед подачей под большим давлением (см. таблицу ниже);
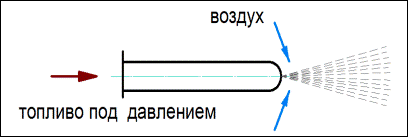
Рис 33.
Когда запускается листовое топливо, центробежная прохождение уменьшается за счет генерируемых сил (см. Рис. 34);
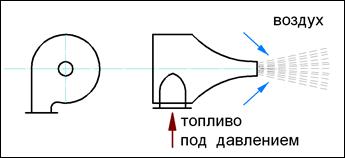
Рис 34. Центрифугальный механический сопло
Вращение компонентов форсунки приводит к тому, что распыление происходит вращательным образом (см. рис. 35).
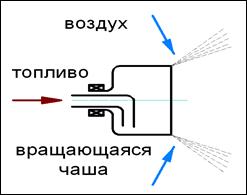
Рис.35. Механическое вращение механического вращения
В механические форсунки поступает мазут под давлением 2,0 МПа. Его вязкость снижается в зависимости от плотности мазута и интенсивности распыления. Перед распылением его нагревают до температуры 90-120 оС (в зависимости от марки) для снижения впитываемости. Под воздействием внешнего давления образующиеся капли подвергаются дополнительному дроблению.
Распылительные форсунки и другие подобные, но более мощные функционирующие трубки высвобождают энергию в основном в результате кинетической энергии движущегося пара или воздуха (см. PLIS 36).
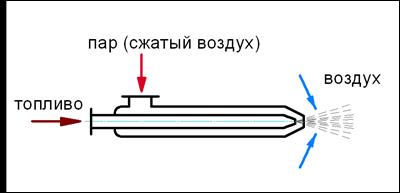
Рис. 36.Десс с аэрозольной средой
При сжигании топливных масел высокое давление производится либо с помощью класса (давление пара p = 0,5 2,5 МПа), украденного воздуха (давление PPA P = 11,5 МПа/кг) или воздуха (сила давления P = 0,44 – 0, 38MP и потреблениеG = 0,35 кг / кг).
10-15% воздуха, используемого в otuchay и air use, который необходим для gopi, поступает мошенническим путем. Воздушная скорость достигает километра в пути 1000 м\с, обеспечивая частое образование капель мазута.
Воздух используется в FOPCKX с низким давлением Cpeed (p = 0,002 0,0007 МПа). В фопкх подается от 50 до 100 % воздуха, что является неприемлемым для говна.
Различие между потребителями энергии топлива под давлением осуществляется с помощью комбинированных форсунок.
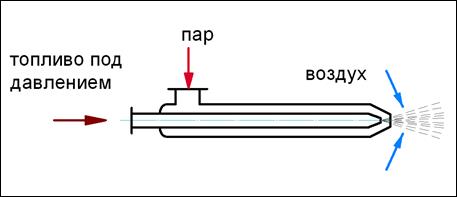
Рис.37. размещенное сопло
Доcтоинства меxаничеких фоpсунок:
Меньше энергии расходуется на личные нужды;
более компактны;
Во время игры 0-я и 3-я скрипки менее шумные;
Не увеличивает увеличение содержания водяного паров продуктов сгорания;
Блики на парнях ярче и имеют более широкий угол вращения.
.
Если мазут загустел слишком сильно, необходима более тонкая очистка;
Меньший распылитель (средний размер капель при давлении топлива Р = 2 МПа составляет 40 микрон; при давлении Р = 1 МПа он составляет около 3 микрон);
Изменение производительности в относительно узком диапазоне (от 80 до 100% против 20,10% у паровых форруннеров).
Для котлов средней и большой мощности, которые обычно непрерывно работают на мазуте.
В установках малой мощности применяются паровые форсунки, которые также используются в качестве пусковых форсунок.
Узкий диапазон ребристости является основой всех недостатков механических форсунок. Этот недостаток устраняется при использовании комбинации пара и механического распыления мазута. Комбинированные форсунки работают как механические форсунки при более низких Rebs и при более высоких нагрузках (менее 60%).
10. Процесс воспламеняемости – это то, что заставляет сжигать твердое топливо.
Сгорание сплошного топлива может быть визуализировано как происходящее на нескольких последовательных этапах. Затем топливо нагревается, и испарение влаги следует. Пирогенное разложение сложных органических соединений и высвобождение летучих веществ начинают происходить при температурах выше 100 ° С. Если окружающая температура выше, чем температура, при которой летучие вещества зажигают, они зажигают и дополнительно нагревают частицу кока -колы до ее мигания. Температура их зажигания уменьшается с увеличением мощности полета.
Тепло окружающих дымовых газов и потери тепла в результате сгорания разлетающихся частиц кокса нагревают. Оба процесса могут происходить одновременно в запыленной среде, поскольку мельчайшие частицы угля нагреваются очень быстро. В реальных обстоятельствах мы имеем дело с полидисперсным составом угольной пыли, где некоторые частицы еще не начали нагреваться, а другие достигли точки выброса.
Чтобы рассчитать общее время сжигания топлива и скорость тепла, важно понять, как сжигает частицу кокса. Тепловая мощность составляет 66% от общего числа, а остаток кокса составляет 55% от веса. Остаток кокса может составить более 96 процентов от сухого начального веса частиц в топливе с очень низкими летучими урожаями (например, золой), а общее количество тепла, выделяемого во время сгорания, составляет всего около 95 процентов.
Сложность этого процесса была продемонстрирована при изучении горения коксового остатка.
При сжигании углерода возможны две первичные реакции прямого гетерогенного окисления
С О2 = СО2 34 МДж/кг ; (14)
2С О2 = 2СО 10,2 МДж/кг . (15)
Образование СО2 и СО приводит к двум последующим реакциям
Оксид углерода 2СО2 12,7 МДж/кг
восстановление диоксида углерода СО2 С = 2СО – 7,25 МДж/кг . (17)
Кроме того, газификация с выделением водорода происходит, когда водяной пар присутствует на нагретой поверхности частицы:
С Н2О = СО Н2 . (18)
Гетерогенные реакции (14, 15 и 17) показывают, что углерод сжигается непосредственно в пламени. Из -за диффузии кислорода из соседнего объема однородная реакция (16) продолжается на поверхности частицы.
Температура газов вблизи поверхности частиц влияет на соотношение CO к CO2. Так, например: реакция распада происходит при 1200 °C.
4С 3О2 = 2СО 2СО2 (Е = 84 ÷ 125 кДж/г-моль),
При температуре выше 1500 С
3С 2О2 = 2СО СО2 (Е = 290 ÷ 375 кДж/г-моль).
Естественно, что при повышении температуры высвобождаемые CO и CO2 выделяются примерно в равном количестве.
В основном, скорость горения определяется двумя факторами:
2) скорость химической реакции, которая подчиняется закону Аррениуса и резко возрастает с повышением температуры;
2) скорости диффузионного или турбулентного подвода кислорода в зону горения.
На ранних стадиях горения, когда температура еще низкая, а скорость химической реакции очень низкая (скорость химического процесса медленнее, чем скорость в окружающем объеме), нет никаких изменений в аэродинамике печи или горелки. Это территория кинетического горения.
В процессе горения выделяется тепло, температура повышается, а скорость химических реакций ускоряется. Затем скорость горения остается постоянной на уровне скорости диффузии воздуха в зону пламени, в то время как концентрация кислорода у поверхности частицы уменьшается. Диффузионное горение – это та область, о которой идет речь.
В переходной области горения скорость диффузии и химических реакций равны.
Скорость переноса кислорода из объема частицы к ее поверхности равна скорости диффузионного перемещения кислорода от поверхности частицы, согласно закону молекулярной диффузии (закону Фика).
, (19)
Где коэффициент диффузионного массообмена
Частичное давление кислорода как на поверхности, так и в объеме.
Скорость химической реакции определяет, какое количество кислорода расходуется вблизи поверхности частицы.
, (20)
где k – константа скорости реакции.
В переходной области, созданной предыдущим государством
,
Откуда берутся лайки
Формула для скорости горения в переходной области потребления окислителя или кислорода может быть получена путем подстановки (21) В (20):
(22)
Где расположена эффективная константа реакции реакции сгорания.
В области относительно низких температур выражение (22) и коэффициент = принимают следующий вид:
,
Кроме того, концентрация кислорода в объеме частицы и на ее поверхности практически одинакова, и скорость горения зависит только от химической реакции.
В экспоненциальном законе Аррениуса говорится, что по мере повышения температуры постоянная скорость химической реакции поднимается (см. Рис. 22), в то время как полученный молекулярно -массовый обмен, 290c, слабый.
.
Коэффициенты e и k становятся соизмеримыми величинами одного порядка, когда скорость потребления кислорода начинает опережать интенсивность его поступления из окружающего объема при определенном значении температуры T*. Процесс переходит в промежуточную (переходную) область горения, когда кривая перегибается. Разница между парциальными давлениями воздуха в объеме и на поверхности также растет одновременно в результате снижения концентрации кислорода вблизи поверхности частицы.
Когда горение усиливается, концентрация кислорода вблизи поверхности почти исчезает, подача воздуха к поверхности существенно не зависит от температуры (k), и процесс смещается в диффузионную область.
.
Интенсифицируя процесс смешивания топлива и воздуха (улучшая устройства для сжигания) или ускоряя проветривание частицы потоком воздуха, можно увеличить скорость горения в диффузионной области.
Большие кучи углекислого газа сжигаются (слоевой метод) вместе с измельченными или газообразными парообразными формами.
Твердые слои при слоевом сжигании будут иметь самую высокую относительную скорость выдувания частиц топлива. Частицы топлива присутствуют в потоке дымовых газов при вихревом и факельном методах сжигания, но их относительная скорость выдувания значительно ниже. В результате должен произойти переход мелких частиц (таких как песчинки) в область диффузии. пыль). Согласно нескольким исследованиям, уголь, взвешенный в потоке газовоздушной смеси, лишь слабо обдувается, а побочные продукты сгорания, которые выходят из него, вызывают образование облака вокруг него. Кроме того, в том, что при факельном методе происходит неоднородное горение пыли, вероятно, виновато значительное увеличение общей реагирующей поверхности. Однако, как и в любом другом очевидном случае, истина не всегда верна.
Законы диффузии определяют поступление кислорода к поверхности. Обобщенная критериальная зависимость между ламинарным потоком и теплообменом небольшой сферической частицы была установлена учеными.
Nu = 2 0,33Re0,5 .
Nu 2 – это скорость мелких частиц для небольших частиц кока -колы (при re 1, что эквивалентно парящей скорости мелких частиц).
.
Поскольку оба они основаны на движении молекул, процесс теплопередачи можно сравнить. В результате законы теплопередачи Фурье и Ньютона-Рихмана имеют аналогичные математические выражения. Из-за формальной аналогии между этими законами и процессами диффузии мы можем использовать в качестве примера следующее:
,
Откуда, (23)
Где D – коэффициент молекулярной диффузии (аналогично тому, как различные процессы имеют различные теплопроводности).
Радиус частиц и коэффициент диффузионного массового переноса (D) обратно связаны в формуле (23). В результате процесс диффузии кислорода на поверхность частицы ускоряется при уменьшении размера частиц топлива. В результате, несмотря на ранее упомянутое снижение скорости выдувных частиц, переход от диффузионного Gorenje к угольной пыли сжигается при более высоких температурах.
Горение частиц кокса смещается из “промежуточной зоны” – зоны диффузии, где важна интенсификация подачи кислорода (Г. Ф. Кнорре и Л. Н. Хитрин, многочисленные экспериментальные и исследовательские работы) [1]; происходит также движение частиц газа через стенки печи на глубину 10 м от поверхности тела с окружающим его электрическим полем: это уменьшает с.
Время горения сферической углеродной частицы в диффузионном поле квадратично зависит от размера частицы:
,
Даны начальный размер частицы, ro, и плотность, h, атома углерода. Do, Po и To (последние три) имеют одинаковый размер (r-размер молекул в топочном объеме, вдали от капли или частицы кислорода). Для каждой стадии горения водорода в течение часа после сжигания топлива без доступа воздуха через газообменную трубку под давлением 1 МПа это означает скорость распространения тепла по трубкам около 10 км/с при температуре выше 100 градусов Цельсия.
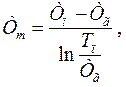
Где – температуры поверхности частицы или окружающих дымовых газов, соответственно Tn и G.
Дата: 2022-07-30;Просмотр 22613
§
В XXI веке наряду с ростом промышленного производства и использования электрической и тепловой энергии увеличилось количество вредных выбросов. Топливо (горючее) потребляется в огромных количествах тепловыми электростанциями, которые выделяют такие продукты сгорания, как:
• золу;
Оксиды азота;
Оксиды серы;
Окись углерода (при недостаточном сгорании топлива);
Углекислый газ (основная причина парникового эффекта).
Двуокись углерода CO2 служит основой для углерода, как и для всех органических топлив (включая ископаемое топливо). Процесс фотосинтеза происходит в природе. Под воздействием солнечного излучения зеленая растительность (деревья, кустарники и т.д.) расщепляет углекислый газ и выбрасывает его в атмосферу. В результате неуклонного роста использования ископаемого топлива нарушился круговорот углекислого газа. В атмосферу выбрасывается большое количество углекислого газа, а наземная растительность уже не в состоянии его поглощать. Только половина из 21,3 Гт CO2, образующегося при сжигании ископаемого топлива каждый год, может быть поглощена естественными процессами.
Количество CO2 в атмосфере Земли поднимается, что вызывает дисбаланс тепла между планетой и атмосферой вокруг нее. Климат на планете постоянно и везде меняется в результате этого дисбаланса. Ученые-климаты впервые определили так называемый парниковый эффект в двадцатом веке.
Границы между государствами не могут остановить “разрыв границ”, поскольку все государства существуют на единой территории. Вообще говоря, проблема сокращения выбросов – не только парниковых, но и всех видов газов – является глобальной. Только 4% мировых выбросов углекислого газа приходится на Россию, и около 25% этих выбросов “перерабатывается” российскими лесами.
В Киотском протоколе изложены строгие правила по сокращению выбросов CO2. Согласно Киотскому протоколу, выбросы CO2 в России не могут быть выше, чем в 1990 году.
Чтобы подготовиться к Рамочной конвенции ООН об изменении климата (РКИК ООН), Киотский протокол – это международное соглашение, которое было принято в декабре 1997 года. Протокол ратифицировали 161 государство, на долю которых в совокупности приходится более 60% глобальных выбросов.
Первым является разработка возобновляемых источников энергии (RES), таких как солнечная энергия, ветер, вода, волны из океана, приливная энергия и геотермальные источники, а также водородное топливо.
В последнее время развитые страны уделяют больше внимания сжиганию так называемого биотоплива, например, древесных гранул.
Конечно, абсолютное количество высвобожденного углерода не изменится, и для выработки необходимого количества тепла потребуется то же количество углерода (если мы говорим о топливе из углекислого газа). Однако дереву требуются миллионы лет, чтобы образовать уголь, пока оно растет и “активно участвует” в фотосинтезе. Относительное количество выбросов CO2 уменьшается при сжигании биотоплива.
Поскольку оксиды азота являются наиболее токсичными, возникает проблема снижения их концентрации в энергетических системах.
Гемикоксид N2O, угарный газ в диоксиде газа водорода и другие азот-кислородные соединения образуются в зависимости от уровня окисления. Существует практическое значение для элементов, обозначенных как «noh». Другие оксиды азота встречаются реже в атмосфере Земли, потому что это нестабильные вещества.
Концентрация конкретного компонента в воздухе играет основную роль в санитарной и гигиенической оценке качества воздуха. Это различает почасовые концентрации и средние, ежемесячные средние значения.
Согласно нормативным документам страны, предельно допустимая концентрация диоксида азота MPKNO2 в России составляет 0,085 мг/м3 по COH 6 на 1 м3. Основным побочным продуктом при сжигании органического топлива является оксид азота, который обычно составляет 2-5% от общего количества углерода жировой ткани. Но поскольку NO в дальнейшем окисляется до более токсичных форм в шлейфе дымовых газов, руководство разрешает пересчитывать концентрацию этих веществ.
Существует три возможных реакции для N O, N2 и PO.
NO О3→NO2 О2; (24)
2 Нет O2 → 2NO2;(25).
Н ЕТ R2 НЕТ R, N O R. (26).
Окисление, также известное как реакция (24), которое преобладает в этих условиях.
Поскольку оксиды азота присутствуют в атмосфере, они оказывают токсическое воздействие как на здоровье человека, так и на здоровье животных и растений. Углекислый газ может оказывать немедленное (до часа) действие, приводящее к пневмонии или бронхиту; при концентрациях 500-1000 мг\/м3 возможен отек легких или смерть.
Оксиды азота и фосфорные кислоты в сочетании с влажностью атмосферы для создания слабых распаков этих кислот. Снижение продуктивности сельского хозяйства, увеличение кислотности водоемов и гибель лесных районов – все это результаты негативного воздействия кислотных дождей. Оксиды азота и серы транспортируются на международном уровне в результате кислотных дождей. В результате национальное решение этой проблемы невозможно.
Снижение прозрачности атмосферы и развитие фотохимического тумана являются дополнительными характеристиками токсического воздействия оксидов азота. Этому явлению особенно подвержены крупные мегаполисы с интенсивным использованием автомобилей и транспорта, а также районы с высокой концентрацией углеводородов.
Согласно российским стандартам, совокупное вредное воздействие оксидов азота и диоксида серы не должно превышать 1, или 1.
. (27)
Нормативные значения выбросов оксидов азота для котельных представлены в таблице 1.
Таблица 1
Максимальные нормы выбросов оксидов азота для котельных установок вступили в силу 1 января 2001 года.
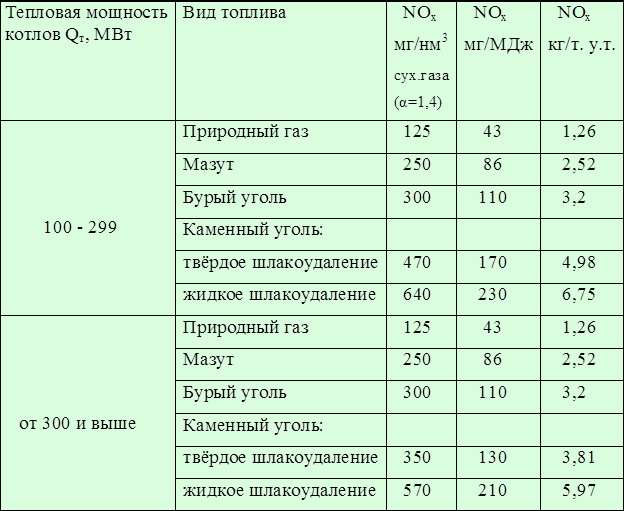
Дата: 2022-07-25;Просмотр 748
§
Стратегии снижения выбросов оксидов азота и аммиака в атмосферу принципиально отличаются друг от друга.
Очистка дымовых газов пассивным методом в специальных установках, размещаемых за котлом, между последним теплоприемником и трубой;
Методический подход к подавлению образования NOX на начальных стадиях.
Это можно выбрать в качестве активной стратегии снижения NOx. Технология очистки дымовых газов признана неэффективной, поскольку она способствует образованию и воспламенению топлива.
Температура и количество кислорода в окружающей среде оказывают влияние на скорость и интенсивность образования NOх.
Температура процесса оказывает лишь незначительное влияние на количество NOx, которое выделяется при сгорании летучих веществ. Зельдович не указал температуру, при которой следует измерять скорость образования NOx.
Оксидов азота для различных видов топлива в котлах. При сжигании природного газа, не содержащего связанного азота, или при отсутствии связанных газов необходимо принимать меры предосторожности для снижения тепловых выбросов оксидов азота. Когда максимальная температура внутри всей топки достигает 1650 градусов Цельсия, при сжигании мазута в высокофорсированных топках, а также когда высококачественный уголь разрушается во время удаления жидкого шлака.
В последнее время было создано множество технических возможностей для снижения концентрации оксидов азота. Основные методы исследования представлены на схеме.
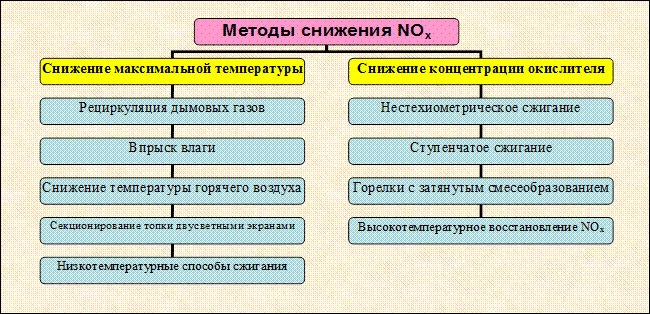
Рис.39. Методы снижения выбросов оксида азота
Рециркуляция газа понижает температуру, тем самым снижая уровень оксидов азота в выхлопных газах. Эффективность рециркуляции газа очень высока, если отсутствуют зависящие от температуры топлива оксиды азота. Выборочно определенные места для введения газов рециркуляции включают канал вторичного воздуха и отверстия под горелками. Тот факт, что этот метод имеет ограниченное применение, объясняется тем, что он улучшает экономические показатели (увеличивает потери дымовых газов и расход электроэнергии при самостоятельном использовании). Для подачи дыма к горелкам необходимо также установить рециркуляционную дымовую трубу и короба.
На стабильность горения и эффективность сжигания угольной пыли может негативно повлиять понижение максимальной температуры путем введения влаги или снижения температуры нагрева воздуха.
Поскольку уменьшение избыточного воздуха является самым простым способом снизить содержание кислорода в вспышке. Делая это, вы используете меньше энергии для ваших собственных потребностей и теряете меньше тепла за счет потери дымохода. Ограничение этого метода объясняется формированием химических продуктов подкрепления при определенном критическом значении G, в зависимости от типа топлива, техники сгорания и конструкции печи или горелки.
В большинстве случаев пылеугольные котлы имеют несколько горелок, расположенных ярусами. Горелки и камера сгорания (топка), следовательно, оказывают влияние друг на друга. Нестехиометрическое сжигание является полезной техникой для сокращения выбросов оксидов азота при многоярусном расположении горелок (рис. 40).
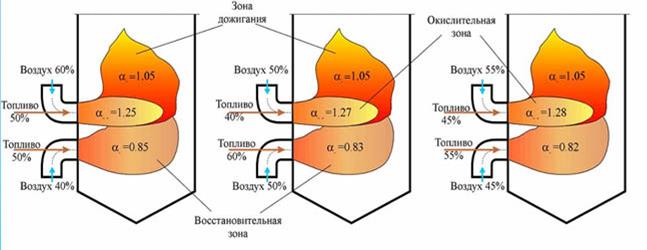
а б в
Рис. 40. Нестехиометрическое сжигание
Асимметрия в воздухе; b симметрия в топливе.
В комбинированном разбалансе:
Отдельные самолеты воздушных затворов покрыты для выполнения нехиометрического сгорания (см. Усилия воздуха на рис. Чтобы предотвратить вступление топлива через отдельные отверстия, 40a) или топливные клапаны перед отдельными горелками, а также ставни из отдельных газовых потоков в печии на уровнях слайдов;Защита специальных воздушных шаров между другими свечами. В обеих ситуациях продукты сгорания смешиваются с окислительными и зонами восстановления для производства топлива с обычным избыточным воздухом. Если комбинированная дисперсия отсутствует (рис. 40 В), то комбинированный символ сдвига также возможно.
Существуют стехиометрическое сжигание и последовательное сжигание. С помощью особых сопел воздух дополнительно навязывается через специальные форсунки внизу (или конец) факела, чтобы обеспечить полное сжигание топлива.
Рис. Двухступенчатый план сжигания показан на рисунке 41.
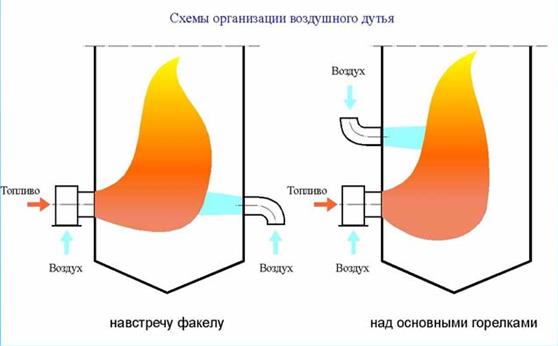
Рис.41
В многоуровневых котлах горелки верхнего яруса могут служить в качестве вторичных дутьевых форсунок (в случае отказа остальных при нормальной нагрузке). Оксиды азота топлива (также известные как горючие) и термические оксиды подавляются на начальном участке пламени, поскольку летучие вещества воспламеняются и горят при пониженной концентрации кислорода. Тепловые оксиды подавляются на втором этапе.
Ступенчатая подача воздуха в окислитель помогает значительно снизить выбросы HNOx. Благодаря ступенчатой подаче воздуха в этой точке углекислый газ окисляется до метана. Чтобы избежать окисления топливного газа при повышенном избытке воздуха в зоне активного горения, оптимальный коэффициент выбросов оксидов азота должен поддерживаться на как можно более низком уровне. Недостаток избытка воздуха может привести к чрезмерному росту концентрации угарного газа и других химических побочных продуктов недогорания.
Трехэтапное сжигание-это разработка процесса сгорания.
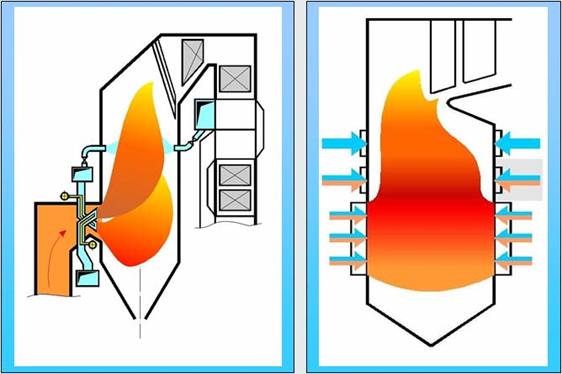
Рис.42. TRT сцены сжигания топлива
Вторая ступень – сжигание при избытке воздуха, близком к единице;
Стадия 2: сгорание происходит при избытке воздуха, который меньше единицы, что снижает оксиды азота стадии 1 до атомной формы углерода;
Третий этап: зона после выживания, где воздух больше, чем в выходе печи.
Дата: 2022-07-30; просмотр-2958
§
Использование уникальных горелок, снижающих выбросы СО, является альтернативным методом снижения выбросов иона азота.
Известно, что стоимость котлов не превышает 2% от общей стоимости котла, поэтому использование специальных конструкций горелок позволяет реализовать ряд технических решений за относительно небольшие деньги.
Конструкция горелки должна включать механизм, снижающий образование оксидов азота:
Чтобы остановить первичную воздушную смесь, которая воспламеняет факел, от включения в нее вторичного воздуха, богатого кислородом;
Для увеличения обмена теплом и массой между двумя воздушными смесями с малым количеством кислорода;
Убедитесь, что топливо эффективно сжигается с наименьшим количеством первичного воздуха;
Привода без ухудшения стабильности зажигания или эффективности выгорания топлива при максимальной температуре ядра сгорания.
Под руководством профессора Р. С. Тюльпанова в Санкт-Петербургском университете промышленной теплоэнергетики была создана горелка, восстанавливающая оксиды азота (рис. 43), и внедрена на Котласском ЦБК.
Два осесимметричных канала служат основой конструкции, позволяя контролировать процессы смешивания и горения. Внешний кольцевой канал подачи вторичного воздуха разделен на два кольца, и суммарная площадь поперечного сечения этих двух колец больше, чем первоначальная площадь поперечного сечения канала вторичного воздуха. В результате скорость потока уменьшается, коэффициент турбулентного обмена уменьшается, а скорость образования смеси увеличивается. В результате на начальном этапе формирования факела содержание кислорода снижается, а окислитель подается ступенчато. “Богатая” смесь окружена третичным кольцевым каналом, который находится несколько ближе к оси горелки.
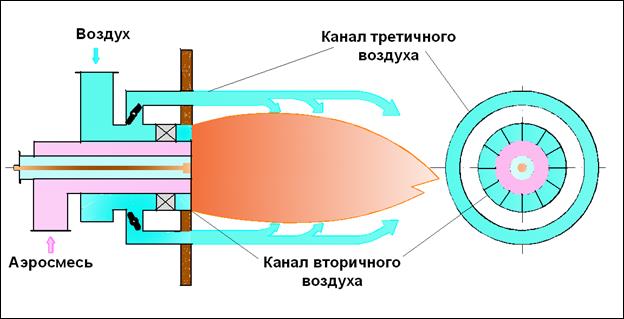
Рис.43. Горелка с затянутым составообразованием
. Используя подобную горелку, которая сочетает в себе принципы подавления и замедленного перемешивания, можно снизить концентрацию азота на 50%.
Методические указания по расчету выбросов оксида азота с дымовыми газами от тепловых электростанций разработаны V TI и МЭИ.
При проектировании новых и реконструкции существующих котельных с производительностью пара от 75 т/ч или гостиничных котельных мощностью до 58 МВт (50 Гкал/ч) и выше, сжигающих твердое жидкое топливо в факельных горелочных устройствах, могут быть использованы методические указания по расчету выбросов оксидов азота.
Дата: 2022-07-30;Просмотр 751
§
Вы привыкли к краткому курсу “Топливо и теория горения”. Почему “краткий” называется “кратким”? Теоретические и практические основы (такие как турбулентное пламя, распространение ламинарного пламени и аэродинамика реактивного движения) не рассматриваются в представленном материале.
Надеюсь, что “знакомство” простирается дальше предисловия и введения. Но даже в этом случае, если вы решите не посещать лекции, вам потребуется значительное количество времени и усилий, чтобы получить более или менее глубокое понимание предлагаемого материала. В лекциях рассматривается “классификация горелок по принципу образования смеси” применительно к виски “Кола” и “кинетическое и диффузионное горение” в качестве иллюстрации из гонок “Формула-1”. Это невозможно объяснить в учебнике.
Поэтому я предлагаю вам посещать лекции. И не просто для того, чтобы что-то зачесть, а для того, чтобы расширить свои знания. Сегодня это еще более актуально, потому что по иронии судьбы (или в результате чьей-то глупости) лекции и практические занятия исчезли. В первый день экзаменационной сессии я уже пожинал первые плоды этой глупости. Студентам, получившим проходной балл на экзамене по математике и литературе у Смирновой, было запрещено посещать занятия.
Конечно, вы можете выделить ключевые вопросы из этой части в каждом параграфе или разделе. Но я именно так и делаю, когда читаю лекции. Количество информации по “Теории горения”, теоретически, безгранично. Однако это невозможно, потому что часть материала предоставляется “для общего развития” или для особо одаренных и любознательных студентов. Даже если такие студенты есть, их не так много.
Информацию нельзя “выучить”, но ее можно понять. Вы должны следовать определенному пути, чтобы не уткнуться лицом в грязь даже через год (и во время работы с фундаментальными идеями на старших курсах).
А вчерашние выпускники, которые до сих пор работают в ТГК-1 или Финляндии, все время просили конспект по курсу “Теория топлива и сгорания”.
Фронтмен The Doors Джим Моррисон однажды заметил, что в мире есть вещи понятные и непонятные, а также все среднее между ними. двери”. Мои дорогие друзья, я призываю вас найти эти двери и впустить непостижимую тьму. Удачи!
Белоусов В. Н
Дата: 2022-07-30;Просмотр 467
Теория расхода воздуха на сжигание газа
На количество вырабатываемого тепла существенно влияет частота и сроки обслуживания газоиспользующего оборудования. Очень важно понимать, что идеальная газовоздушная смесь обеспечивает гарантию безопасности. Давайте обсудим расход воздуха для сжигания газа более подробно.
Метан, основной компонент природного газа, можно сжечь, используя всего две молекулы кислорода. Для окисления кубического метра топлива потребуется вдвое больше кислорода, выраженного в понятных объемах.
Однако в реальных условиях все гораздо сложнее. Воздух, из которого кислород составляет лишь одну пятую часть, служит окислителем в химической физике горения. Его доля составляет ровно 20,93%. Следовательно, потребуется в 9,52 раза больше воздуха.
Если вы выполните следующие два действия, то сможете определить цифру:
- Деление 100/21. С помощью этой операции мы можем узнать, что воздуха в объеме в 4,76 раза больше, чем кислорода.
- Умножение 4,76 на 2 дает 9,52, то есть ровно во столько раз больше воздуха, сколько необходимо для сжигания любого количества природного газа.
Теоретический расход – это расчетное количество воздуха, необходимое для эффективного сжигания газа. Gorenje, но на самом деле вы найдете это полезным. Расчет был произведен при идеальных обстоятельствах, и почти всегда существует ряд переменных, которые могут вызвать существенные изменения.
Они включают в себя:
- Состав и качество реагентов (воздух, газ);
- Тип оборудования, используемого для подачи энергии;
- Состояние оборудования;
- Способ подачи газа и воздуха, а также ряд других моментов.
Вышеупомянутые характеристики иногда могут приниматься во внимание, если требуется особая точность. Точный состав газа можно определить в ближайшем представительстве газовой службы. Значение 9-52 просто умножается на коэффициент избытка воздуха, когда точность не требуется. чье значение обычно находится в диапазоне от 1,1 до 2; и чье значение обычно находится в диапазоне от 1,2 до 1,5.
Если требуется точность, то количество фактически использованного воздуха следует разделить на теоретический расход, рассчитанный в ходе расчета. Однако обычно предпочтительнее использовать среднее значение коэффициента избытка воздуха.
Так что же он равен?
- Необходимо в 1,1 – 10,472 раза больше массы воздуха;
- В 1,4 – 13,328 раза больше воздуха
Для сжигания каждого кубического метра топлива потребуется до 13 328 м3 воздуха.








