- Круговорот в природе
- Особые режимы горенияПравить
- Горение в пористой среде
- Углекислый газ в природе
- Состав
- Углекислый газ
- Оксид углерода
- Вода
- Цианистый водород
- Акролеин
- Формальдегид
- Азотсодержащие вещества
- Сернистый газ
- Дым
- Пепел, зола, копоть, сажа, уголь
- Первая помощь при отравлении
- Классификация видов горенияПравить
- Определение оксида углерода(II)Править
- Историческая справкаПравить
- Оксид углерода(II) в атмосфере ЗемлиПравить
- Открытие
- Горение газа. Реакции горения газообразного топлива.
- ПламяПравить
- Электрические свойства пламени
- Взаимодействие с другими веществами
- История открытияПравить
- Классификация
- Оксид углерода(II) в космическом пространствеПравить
- Взаимодействие углекислого газа с веществами и его химические свойства
- Гетерогенное горениеПравить
Круговорот в природе
Организмам и растениям для поддержания жизненных процессов необходим углерод, круговорот которого в углеродном цикле планеты осуществляется двуокисью углерода. Регулирование концентрации CO2, с конца докембрийского периода (540 млн. лет назад) и до начала индустриально-промышленной эпохи, производится происходящими в земной коре геологическими процессами и производящими фотосинтез организмами. Одни из них образуют и выбрасывают, другие поглощают и вдыхают.
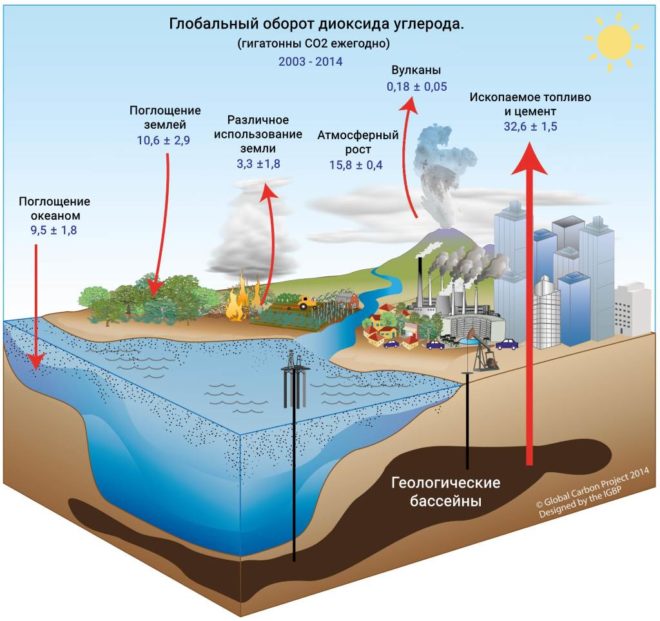
Энергия света, попадая на растительные организмы, водоросли и некоторые виды бактерий, активирует процессы, производящие сложные органические соединения (углеводы) из простых неорганических (CO2 и вода). При этом кислород образуется в качестве побочного продукта. Двуокись углерода также является побочным продуктом организмов, для дыхания которым необходим кислород. Газ попадает в воду через жабры рыб и в воздух через легкие людей и животных. Углекислый газ появляется в результате распада органики (гниение) и в процессе брожения. Вулканы производят выброс углекислого газа, океаны осуществляют его поглощение. Сжигая дрова и другие органические материалы, ископаемые виды топлива, также происходит выделение углекислоты.
Особые режимы горенияПравить
Инфракрасная газовая печка с пористыми матрицами в качестве нагревательных элементов
Горение в пористой среде
Углекислый газ в природе
Углекислый газ в природе образуется из различных источников:
- Дыхание животных и растений. Каждому школьнику известно, что растения поглощают углекислый газ CO2 из воздуха и используют его в процессах фотосинтеза. Некоторые хозяйки пытаются обилием комнатных растений искупить недостатки приточной вентиляции. Однако растения не только поглощают, но и выделяют углекислый газ в отсутствие света – это часть процесса дыхания. Поэтому джунгли в плохо проветриваемой спальне – не очень хорошая идея: ночью уровень CO2 будет расти еще больше.
- Вулканическая деятельность. Диоксид углерода входит в состав вулканических газов. В местностях с высокой вулканической активностью CO2 может выделяться прямо из земли – из трещин и разломов, называемых мофетами. Концентрация углекислого газа в долинах с мофетами столь высока, что многие мелкие животные, попав туда, умирают.
- Разложение органических веществ. Углекислый газ образуется при горении и гниении органики. Объемные природные выбросы диоксида углерода сопутствуют лесным пожарам.
Углекислый газ «хранится» в природе в виде углеродных соединений в полезных ископаемых: угле, нефти, торфе, известняке. Гигантские запасы CO2 содержатся в растворенном виде в мировом океане.

Выброс углекислого газа из открытого водоема может привести к лимнологической катастрофе, как это случалось, например, в 1984 и 1986 гг. в озерах Манун и Ньос в Камеруне. Оба озера образовались на месте вулканических кратеров – ныне они потухли, однако в глубине вулканическая магма все еще выделяет углекислый газ, который поднимается к водам озер и растворяется в них. В результате ряда климатических и геологических процессов концентрация углекислоты в водах превысила критическое значение. В атмосферу было выброшено огромное количество углекислого газа, который наподобие лавины спустился по горным склонам. Жертвами лимнологических катастроф на камерунских озерах стали около 1 800 человек.
Состав
Состав их зависит от состава горящего вещества и условий его горения. В условиях пожара чаще всего горят органические вещества (древесина, ткани, бензин, керосин, резина и др.), в состав которых входят главным образом углерод, водород, кислород и азот. При горении их в достаточном количестве воздуха и при высокой температуре образуются продукты полного сгорания: СО2, Н2О, N2. При горении в недостаточном количестве воздуха или при низкой температуре кроме продуктов полного сгорания образуются продукты неполного сгорания: СО, С (сажа).
Продукты сгорания называют влажными, если при расчете их состава учитывают содержание паров воды, и сухими, если содержание паров воды не входит в расчетные формулы.
Реже во время пожара горят неорганические вещества, такие как сера, фосфор, натрий, калий, кальций, алюминий, титан, магний и др. Продуктами сгорания их в большинстве случаев являются твердые вещества, например Р2О5, Na2O2, CaO, MgO. Образуются они в дисперсном состоянии, поэтому поднимаются в воздух в виде плотного дыма. Продукты сгорания алюминия, титана и других металлов в процессе горения находятся в расплавленном состоянии.
При неполном сгорании органических веществ в условиях низких температур и недостатка воздуха образуются более разнообразные продукты – окись углерода, спирты, кетоны, альдегиды, кислоты и другие сложные химические соединения. Они получаются при частичном окислении как самого горючего, так и продуктов его сухой перегонки (пиролиза). Эти продукты образуют едкий и ядовитый дым. Кроме того, продукты неполного горения сами способны гореть и образовывать с воздухом взрывчатые смеси. Такие взрывы бывают при тушении пожаров в подвалах, сушилках и в закрытых помещениях с большим количеством горючего материала. Рассмотрим кратко свойства основных продуктов горения.
Углекислый газ
Углекислый газ или двуокись углерода (СО2) – продукт полного горения углерода. Не имеет запаха и цвета. Плотность его по отношению к воздуху равна 1,52. Плотность углекислого газа при температуре Т = 0С и при нормальном давлении р = 760 миллиметров ртутного столба (мм Hg) равна 1,96 кг/м3 (плотность воздуха при этих же условиях равна ρ = 1,29 кг/м3). Углекислый газ хорошо растворим в воде (при Т = 15 °С в одном литре воды растворяется один литр газа). Углекислый газ не поддерживает горение веществ, за исключением щелочных и щелочно-земельных металлов. Горение магния, например, происходит в атмосфере углекислого газа по уравнению:
CO2 +2 Mg = C + 2 MgO.
Токсичность углекислого газа незначительна. Концентрация углекислого газа в воздухе 1,5 % безвредна для человека длительное время. При концентрации углекислого газа в воздухе, превышающей 3-4,5 %, нахождение в помещении и вдыхание газа в течение получаса опасно для жизни. При температуре Т = 0 °С и давлении р = 3,6 МПа углекислый газ переходит в жидкое состояние. Температура кипения жидкой углекислоты составляет Т = –78 °С. При быстром испарении жидкой углекислоты газ охлаждается и переходит в твердое состояние. Как в жидком, так и твердом состоянии, капли и порошки углекислоты применяются для тушения пожаров.
Оксид углерода
Оксид углерода или угарный газ (СО) – продукт неполного сгорания углерода. Этот газ не имеет запаха и цвета, поэтому особо опасен. Относительная плотность равна 0,97. Плотность угарного газа при Т = 0 °С и р = 760 мм Hg составляет 1,25 кг/м3. Этот газ легче воздуха и скапливается в верхней части помещения при пожарах. В воде оксид углерода почти не растворяется. Способен гореть и с воздухом образует взрывчатые смеси. Угарный газ при горении дает пламя синего цвета. Угарный газ является очень токсичным. Вдыхание воздуха с концентрацией угарного газа 0,4 % смертельно для человека. Стандартные противогазы от угарного газа не защищают, поэтому при пожарах применяются специальные фильтры или кислородные изолирующие приборы.
Вода
Всем известная вода – Н2О – также выделяется во время горения виде газа – как пар. Вода является продуктом горения газа метана – СН4. Вообще, вода и углекислота в основном выделяются при полном сгорании всех органических веществ.
Цианистый водород
Цианистый калий – сильнейший яд – соль синильной кислоты, также известной как цианистый водород – HCN. Это бесцветная жидкость, но очень летучая (легко переходящая в газообразное состояние). То есть при горении она тоже будет выделяться в атмосферу в виде газа. Синильная кислота очень ядовита, даже небольшая – 0,01 процент – концентрация в воздухе приводит к летальному исходу. Отличительной чертой кислоты является характерный запах горького миндаля. Но синильной кислоте присуща одна «изюминка» – отравиться ей можно, не только вдыхая непосредственно органами дыхания, но и через кожу. Так что защититься только средствами индивидуальной защиты органов дыхания и зрения не получится.
Акролеин
Пропеналь, акролеин, акрилальдегид – все это названия одного вещества, ненасыщенного альдегида акриловой кислоты: СН2=СН-СНО. Этот альдегид тоже является сильно летучей жидкостью. Акролеин бесцветен, с резким запахом, очень ядовит. При попадании жидкости или ее паров на слизистые, особенно в глаза, вызывает сильное раздражение. Пропеналь является высокореакционным соединением, и это объясняет его высокую токсичность.
Формальдегид
Подобно акролеину, формальдегид принадлежит к классу альдегидов и является альдегидом муравьиной кислоты. Также это соединение известно как метаналь. Это токсичный, бесцветный газ с резким запахом.
Азотсодержащие вещества
Чаще всего во время горения веществ, содержащих азот, выделяется чистый азот – N2. Этот газ и так содержится в атмосфере в большом количестве. Азот может быть примером продукта горения аминов. Но при термическом разложении, к примеру, солей аммония, а в некоторых случаях и при самом горении, в атмосферу выбрасываются и его оксиды, со степенью окисления азота в них плюс один, два, три, четыре, пять. Оксиды – газы, имеют бурый цвет и чрезвычайно токсичны.
Сернистый газ
Сернистый газ (SO2) – продукт горения серы и сернистых соединений. Бесцветный газ с характерным резким запахом. Относительная плотность сернистого газа равна 2,25. Плотность этого газа при Т = 0 °С и р = 760 мм Hg составляет 2,9 кг/м3, то есть он намного тяжелее воздуха. Сернистый газ хорошо растворяется в воде, например, при температуре Т = 0 °С в одном литре воды растворяется восемьдесят литров SO2, а при Т = 20 °С – сорок литров. Сернистый газ горение не поддерживает. Действует раздражающим образом на слизистые оболочки дыхательных путей, вследствие чего является очень токсичным.
Дым
При горении многих веществ, кроме рассмотренных выше продуктов сгорания выделяется дым – дисперсная система, состоящая из мельчайших твердых частиц, находящихся во взвешенном состоянии в каком-либо газе. Диаметр частиц дыма составляет от 10−4 до 10−6 см (от 1 до 0,01 мкм). Отметим, что 1 мкм (микрон) равен 10−6 м или 10−4 см. Более крупные твердые частицы, образующиеся при горении, быстро оседают в виде копоти и сажи. При горении органических веществ дым содержит твердые частицы сажи, взвешенные в CO2, CO, N2, SO2 и других газах. В зависимости от состава и условий горения вещества получаются различные по составу и по цвету дымы. При горении дерева, например, образуется серовато-черный дым, ткани – бурый дым, нефтепродуктов – черный дым, фосфора – белый дым, бумаги, соломы – беловато-желтый дым.
В составе дыма, образующегося на пожарах при горении органических веществ, кроме продуктов полного и неполного сгорания, содержатся продукты термоокислительного разложения горючих веществ. Образуются они при нагреве еще негорящих горючих веществ, находящихся в среде воздуха или дыма, содержащего кислород. Обычно это происходит перед факелом пламени или в верхних частях помещений, где находятся нагретые продукты сгорания.
Состав продуктов термоокислительного разложения зависит от природы горючих веществ, температуры и условий контакта с окислителем. Так, исследования показывают, что при термоокислительном разложении горючих веществ, в молекулах которых содержатся гидроксильные группы, всегда образуется вода. Если в составе горючих веществ находятся углерод, водород и кислород, продуктами термоокислительного разложения чаще всего являются углеводороды, спирты, альдегиды, кетоны и органические кислоты. Если в составе горючих веществ, кроме перечисленных элементов, есть хлор или азот, то в дыме находятся также хлористый и цианистый водород, оксиды азота и другие соединения. Так, в дыме при горении капрона содержится цианистый водород, при горении линолеума «Релин» – сероводород, диоксид серы, при горении органического стекла – оксиды азота. Продукты неполного сгорания и термоокислительного разложения в большинстве случаев являются токсичными веществами, поэтому тушение пожаров в помещениях производят только в кислородных изолирующих противогазах.
Пепел, зола, копоть, сажа, уголь
Копоть, или сажа – остатки углерода, который не вступил в реакцию, по разным причинам. Сажу называют также амфотерным углеродом. Зола, или пепел – мелкие частицы неорганических солей, не сгоревших или не разложившихся при температуре горения. При выгорании топлива эти микросоединения переходят во взвешенное состояние или скапливаются внизу. А уголь – это продукт неполного сгорания дерева, то есть не сгоревшие его остатки, но при этом еще способные гореть. Конечно, это далеко не все соединения, которые выделятся при сгорании тех или иных веществ. Перечислить их всех нереально, да и не нужно, потому что другие вещества выделяются в ничтожно малых количествах, и только при окислении определенных соединений.
Первая помощь при отравлении
Симптомы интоксикации разными веществами могут отличаться, но принципы оказания первой помощи всегда одинаковые.
Большинство ядов поступает через дыхательные пути. Первое, что необходимо сделать при отравлении – прекратить поступление продуктов горения в организм. Для этого необходимо:
- соблюдая безопасность и если имеется такая возможность прекратить поступление токсичного вещества – газа, дыма;
- проветрить помещение или иной объем где находится пострадавший;
- снять загрязнённую одежду;
- при отсутствии противопоказаний перенести пострадавшего в безопасное место.
Острая интоксикация требуют оказания экстренной помощи. Действия при отравлении продуктами горения, следующие:
- вызвать «скорую помощь»;
- при задымлении предусмотреть способы защиты органов дыхания от продуктов горения;
- если есть симптомы раздражения – промыть глаза, полость рта, носа;
- при отсутствии сознания придать пострадавшему горизонтальное положение и обеспечить проходимость дыхательных путей;
- до приезда медицинских специалистов наблюдать за сознанием, дыханием, частотой сердечных сокращений, артериальным давлением;
- если есть признаки терминального состояния, то приступить к сердечно-лёгочной реанимации.
Некоторые ингаляционные отравления продуктами горения имеют период мнимого благополучия. Даже при отсутствии патологических симптомов, стоит внимательно следить за состоянием тех, кто может быть отравлен. При первых же признаках неблагополучия необходимо вызывать соответствующих специалистов.
Отравление продуктами горения у детей развивается быстрее, чем у взрослых. Это объясняется более высоким уровнем кислородного обмена. У малышей появляются жалобы на головную боль, сонливость, слезотечение, тошноту. При осмотре заметны изменения цвета кожи, учащение и затруднение дыхания, нарушения координации. Принципы оказания первой помощи для детей те же, что и для взрослых. При отсутствии специализированной медицинской помощи, пострадавшему ребенку угрожают необратимые изменения центральной нервной системы.
Классификация видов горенияПравить
Выделяют также такие особые виды горения, как тление, беспламенное и холоднопламенное горение.
Определение оксида углерода(II)Править
Качественно можно определить наличие CO по потемнению растворов хлорида палладия (или пропитанной этим раствором бумаги). Потеменение связано с выделением мелкодисперсного металлического палладия по схеме:
Эта реакция очень чувствительная. Стандартный раствор: 1 грамм хлорида палладия на литр воды.
Количественное определение оксида углерода(II) основано на иодометрической реакции:
Историческая справкаПравить
Жёлтый цвет пламени газовой горелки при внесении в него следов натрия (поваренная соль на проволоке) вызван излучением дублетной D-линии натрия с длинами волн 589 и 589,6 нм
До открытия кислорода в начале 1770-х годов Карлом Шееле и Джозефом Пристли считалось, что все тела, способные гореть, содержат особое начало, «флогистон», которое в процессе горения выделяется из тела, оставляя золу. В 1775 году Лавуазье показал, что напротив, к горючему веществу при горении присоединяется кислород воздуха, а в 1783 году Лавуазье и Лаплас обнаружили, что продукт горения водорода — чистая вода. Эти открытия заложили основу современных научных взглядов на природу горения.
Все эти работы стали классическими в теории горения.
Оксид углерода(II) в атмосфере ЗемлиПравить
Содержание CO в атмосфере Земли по данным MOPITT
Различают природные и антропогенные источники поступления в атмосферу Земли. В естественных условиях, на поверхности Земли, CO образуется при неполном анаэробном разложении органических соединений и при сгорании биомассы, в основном в ходе лесных и степных пожаров. Оксид углерода(II) образуется в почве как биологическим путём (выделение живыми организмами), так и небиологическим. Экспериментально доказано выделение оксида углерода(II) за счёт обычных в почвах фенольных соединений, содержащих группы OCH3 или OH в орто- или пара-положениях по отношению к первой гидроксильной группе.
Общий баланс продуцирования небиологического CO и его окисления микроорганизмами зависит от конкретных экологических условий, в первую очередь от влажности и значения pH. Например, из аридных почв оксид углерода(II) выделяется непосредственно в атмосферу, создавая таким образом локальные максимумы концентрации этого газа.
В атмосфере СО является продуктом цепочек реакций с участием метана и других углеводородов (в первую очередь, изопрена).
Основным антропогенным источником CO в настоящее время служат выхлопные газы двигателей внутреннего сгорания. Оксид углерода образуется при сгорании углеводородного топлива в двигателях внутреннего сгорания при недостаточных температурах или плохой настройке системы подачи воздуха (подается недостаточное количество кислорода для окисления CO в CO2). В прошлом значительную долю антропогенного поступления CO в атмосферу обеспечивал светильный газ, использовавшийся для освещения помещений в XIX веке. По составу он примерно соответствовал водяному газу, то есть содержал до 45 % оксида углерода(II). В коммунальной сфере не применяется в виду наличия значительно более дешёвого и энергоэффективного аналога — природного газа.
Поступление CO от природных и антропогенных источников примерно одинаково.
Открытие

Первооткрывателем углекислого газа является шотландский физик и химик, Джозеф Блэк (Joseph Black). В 1756 году ученный проводил эксперимент, нагревая белую магнезию (MgCO3). В результате нагрева он выявил, что карбонат магния разложился до жженой магнезии (оксида магния) с потерей массы и образованием так называемого «связанного воздуха». Этим воздухом, как не трудно догадаться, был диоксид углерода.

Впервые, при детальном изучении CO2, Джозеф Блэк доказал что, окружающий нас воздух, это не единая субстанция, а смесь газов. До этого момента все ученные считали воздух одним газом.
Горение газа. Реакции горения газообразного топлива.
Горение – это процесс быстрого окисления С и Н топлива, сопровождаемый выделением тепла, света и продуктов сгорания.
Реакции горения описываются стехиометрическими уравнениями, характеризующими качественные и количественные стороны реакции до ее начала и после завершения.
При горении в воздухе учитывают, что соотношение между азотом и кислородом N2/O2=79/21=3,76.
Общая формула горения углеводора:
Из этого выражения следует, что при сжигании 1-го нормального м 3 углеводорода CnHm требуется (n+m/4) нормального м 3 кислорода и 4,76 (n+m/4) нормального м 3 воздуха.
Определение количества воздуха необходимого для сжигания газа и выход продуктов сгорания
Т.е. для сжигания 1 м 3 газа CnHmтребуется (n+m/4) м 3 кислорода или 4,76(n+m/4) м 3 воздуха.Таким образом для природного газа, в составе которого отсуствуетCO и Н2 количество кислорода необходимого для сжигания газа может быть определено по выражению:
А теоретическое количество воздуха
CnHm-объёмное содержание углеводородов входящих в состав газовой смеси.
При влажном воздухе:
dв–влагосодержание воздуха) г/м 3 .
Трубочные процессы ведутся с некоторым избытком воздуха, поэтому действительное количество воздуха определяют:
В состав продуктов сгорания входят углекислый газ, водяные пары, азот, кислород, иногда SO2. Их количество определяется стехиометрическими уравнениями горения.
Количество CO2 образ. При сгорании 1 м 3 газообр. Топлива зависит отсодержание углерода в компонентах смеси и в балласте топлива:
CO2 ,CO- объёмные доли(в процентах) содержания углекислого газа и окиси углерода в смеси.
При наличии в газообр. Топливе сероводорода в состав продуктов сгорания входит сернистый ангидрид(SO2)
H2S-объёмное содержание сероводорода в смеси.
Количество образующихся водяных паров слагается из V паров, получаемых в результате сгорания водорода, входящего в углеводород, и из других соединений водяных паров, содержащихся в газ Топливе в виде балласта и поступивших с воздухом.
H2-объёмное содержание водорода в топливе
dг-влагосодержание газа г/м 3
Количество кислорода входящее в состав продуктов сгорания определяется коэффициентом избытка воздуха, при котором ведётся процесс горения.
Содержание азота также определяется коэффициентом избытка воздуха и наличием азота в балласте топлива:
N2-объёмное содержание азота в газоаом топливе.
Полный объём продуктов сгорания 1 м 3 газообр. Топлива составит:
Температуры горения газа.
Основное количество тепла, выделяющегося при сжигании газа расходуется на нагрев продуктов сгорания до определённой температуры.
Различают следующие температуры горения газов:
Жаропроизводительность — это t продуктов полного сгорания горючих газов в адиабатических условиях при α=1 и при первоначальной t газа и воздуха = 0 0 С.
iпр. сгор-теплосодержание продуктов сгорания кДж/м 3
tж-жаропроизводительность, 0 С.
Vco2 VН20 VN2 –объем сотавных частей продуктов сгорания 1 м 3 газа.
Ср –средняя объёмная теплоёмкость при P=const. составных частей продуктов сгорания.
В формуле используется средняя теплоёмкость, так как Ср- величина непостоянная, растёт с повышением температуры.
tж:для метана 2043 0 С ; для пропана 2110 0 С ; для водорода 2235 0 С
Эти данные при горении в сухом воздухе.
При содержании 2 % по массе влаги температура понижается на 25-30 0 С
Калориметрическая- t горения газа, учитывающая коэф. Избытка воздуха и физическое тепло газа и воздуха, т.е принимается действительные значения тем-ры. другими словами это t до которой нагрелись бы продукты полного сгорания, если бы всё тепло топлива и воздуха пошло на их нагрев.
iгiв- энтальпия газа и воздуха кДж/м 3
Написав уравнение в развёрнутом виде и решив его относительно калорим. тем-ры Получим:

Tг tв –исходная темпетатура газа и воздуха.
 — расход газа,
— расход газа,
 теоретическое количество воздуха необходимое для сжигания 1 метра куб. газа.
теоретическое количество воздуха необходимое для сжигания 1 метра куб. газа.
Физическое тепло газа и воздуха следует учитывать, если они перед сжиганием нагреты свыше 100 0 C, так как при меньших t эта величина незначительна по сравнению с теплотой сгорания.
Теоретическая температура горения учитывает потери тепла за счёт химической неполноты сгорания и при эндотермических реакциях диссоциации продуктов сгорания.
Qx- потери теплоты за счёт химической неполноты сгорания и на диссациацию СО2 и Н20.
При t до 1500 0 C(имеет место в топках котлов и пром. Печей) величину Qx можно не учитывать так как в этом случае диссоциирует ничтожная доля продуктов сгорания. При более высоких температурах надо учитывать.).
Действительная темература горения достигается в реальных условиях сжигания топлива, она ниже теоретической, так как при ее определении учитываются теплопотери в окружающую среду, длительность процесса горения, метод сжигания газа и другие факторы.
ηп—опытный пирометрический коэффициент .Для большинства топок котлов и печей 0,65. Для наиболее совершенных 0,8- 0,85


Живите по правилу: МАЛО ЛИ ЧТО НА СВЕТЕ СУЩЕСТВУЕТ? Я неслучайно подчеркиваю, что место в голове ограничено, а информации вокруг много, и что ваше право.

ЧТО ТАКОЕ УВЕРЕННОЕ ПОВЕДЕНИЕ В МЕЖЛИЧНОСТНЫХ ОТНОШЕНИЯХ? Исторически существует три основных модели различий, существующих между.

ЧТО И КАК ПИСАЛИ О МОДЕ В ЖУРНАЛАХ НАЧАЛА XX ВЕКА Первый номер журнала «Аполлон» за 1909 г. начинался, по сути, с программного заявления редакции журнала.

Что делать, если нет взаимности? А теперь спустимся с небес на землю. Приземлились? Продолжаем разговор.
Не нашли то, что искали? Воспользуйтесь поиском гугл на сайте:
ПламяПравить
Пламя в горелке Бунзена. 1 — подача воздуха закрыта; 2 — подача воздуха снизу почти перекрыта; 3 — смесь близка к стехиометрической; 4 — максимальная подача воздуха
В зоне горения могут возникать свободные радикалы и молекулы в электронно-возбуждённых и колебательно-возбуждённых состояниях. Если интенсивность свечения достаточно высока, то его можно воспринимать невооружённым глазом. Цвет пламени определяется тем, на каких частотах идут квантовые переходы, вносящие основной вклад в излучение в видимой области спектра. Значительная часть излучения, особенно при наличии твёрдой фазы, пылинок или частиц сажи в пламени, приходится на инфракрасную область, которая субъективно воспринимается как жар от огня. В инфракрасное излучение вносят вклад колебательно-возбуждённые молекулы CO, CO2 и H2O.
Способность примесей окрашивать пламя в различные цвета используется в аналитической химии для пирохимического анализа и в пиротехнике для салютов, фейерверков и сигнальных ракет.
Электрические свойства пламени
Взаимодействие с другими веществами
Углекислота относится к кислотным оксидам, то есть в сочетании с водой образуется кислота. Однако угольная кислота неустойчива и распадается сразу. Эта реакция имеет обратимый характер:
СО2 + H2O ↔ CO2 × H2O (растворение) ↔ Н2СО3
Диоксид углерода + вода ↔ угольная кислота
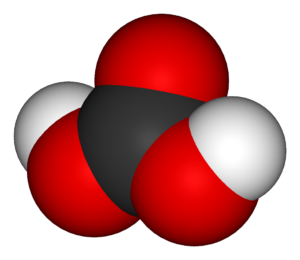
При взаимодействии углекислого газа и соединений азота с водородом (аммиаком) в водном растворе происходит разложение до углеаммонийной соли.
2NH3 + CO2 + H2O = NH4HCO3
Аммиак + углекислота = гидрокарбонат аммония

Полученное вещество часто используется в приготовлении хлеба и различных кондитерских изделий.
Ход некоторых реакций должен поддерживаться высокими температурами. Примером является производство мочевины при 130 °C и давлении 200 атм., схематически изображаемое так:
Также под воздействием температуры около 800 градусов протекает реакция образования оксида цинка:

Возможно уравнение с гидроксидом бария, при котором выделяется средняя соль.
Ba(OH)2+CO2 = BaCO3 + H2O
Гидроксид бария + углекислота = карбонат бария + оксид водорода.
Применяется для регулировки калориметров по теплоемкости. Также вещество используют в промышленности для производства красных кирпичей, синтетических тканей, фейерверков, гончарных изделий, плитки для ванн и туалетов.
Углекислый газ выделяется при реакциях горения.

Метан + кислород = углекислота + вода (в газообразном состоянии) + энергия
Этилен + кислород = диоксид углерода + оксид водорода + энергия
Этан + кислород = двуокись углерода + вода + энергия
C2H5OH + 3O2 = 3H2O + 2CO2 + Q
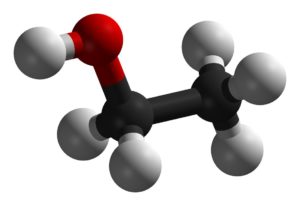
Этанол + кислород = вода + углекислота + энергия
Газ не поддерживает горения, этот процесс возможен только с некоторыми активными металлами, например, магнием.
2Mg + CO2 = C + 2MgO
Магний + углекислота = углерод + оксид магния.
MgO активно применяется при производстве косметических средств. Вещество используют в пищевой промышленности как пищевую добавку.
Двуокись углерода реагирует с гидроксидами с получением солей, которые существуют в двух формах, как карбонаты и бикарбонаты. Например, углекислый газ и гидроксид натрия, согласно формуле, образуют гидрокарбонат Na:
Или же при большем количестве NaOH образуется карбонат Na с образованием воды:
Кислотно-щелочные реакции углекислоты используются на протяжении веков для затвердевания известкового раствора, что может быть выражено простым уравнением:

В зелёных растениях играет важную роль в процессе фотосинтеза:
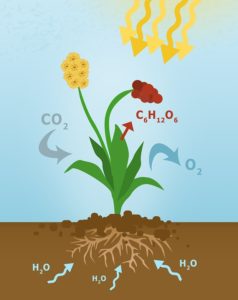
Химические свойства углекислоты используются в промышленности при производстве соды, суть этого процесса можно выразить суммарным уравнением:
Фенолят Na разлагается при взаимодействии с углекислым газом, при этом малорастворимый фенол выпадает в осадок:
C6H5ONa + CO2 + H2O = C6H5OH + NaHCO3
Фенолят натрия + двуокись углерода + оксид водорода = фенол + гидрокарбонат натрия
Пероксид натрия и углекислый газ, взаимодействуя, образуют среднюю соль карбоната Na с выделением кислорода.

Образование углекислоты происходит при растворении в воде кальцинированной соды (стиральной соды).
CO2 вступает в реакцию с гидроксидом калия, последний образуется путем электролиза хлористого калия.
Газ в силу своего строения не реагирует с благородными газами, то есть гелием, неоном, аргоном, криптоном, ксеноном, радоном, оганесоном.
История открытияПравить
Токсичность дыма, выделяющегося при горении угля, была описана ещё Аристотелем и Галеном.
Оксид углерода(II) был впервые получен французским химиком Жаком де Лассоном в 1776 году при нагревании оксида цинка с углём, но первоначально его ошибочно приняли за водород, так как он сгорал синим пламенем.
Классификация
Большинство продуктов горения являются отравляющими веществами. Поэтому, говоря об их классификации, будет правильным ознакомить вас со следующим термином:
Классификация опасности веществ по степени воздействия на организм – это установление (ранжирование) уровней опасности веществ по их поражающему и повреждающему воздействию на организм человека и (или) животного. Более подробно о данной классификации читайте в материале по ссылке >>
Также ознакомьтесь с познавательным материалом по теме:
Токсичность продуктов горения
Показатель токсичности продуктов горения
Оксид углерода(II) в космическом пространствеПравить
Взаимодействие углекислого газа с веществами и его химические свойства

Общие химические свойства углекислого газа: CO2 инертен, то есть химически не активен; при попадании в водный раствор легко вступает в реакции.
Большинство кислотных оксидов устойчивы к высоким температурам, но углекислота при их воздействии восстанавливается.
Гетерогенное горениеПравить
Гетерогенное горение чрезвычайно важно в практических приложениях горения. Большинство топлив удобнее хранить и транспортировать в жидком виде (в том числе сжиженный природный газ). Рабочие процессы в топках, двигателях внутреннего сгорания, дизельных двигателях, воздушно-реактивных двигателях, жидкостных ракетных двигателях — это гетерогенное горение, а оптимизация процесса испарения и смешения топлива и окислителя для их подачи в камеру сгорания — важная составная часть оптимизации всего процесса горения в рабочих системах.
Практически все пожары — это также гетерогенное горение, однако взрывы бытового газа относятся к гомогенному горению, так как исходно и горючее, и окислитель — это газы.








